微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (16分)某小组的同学对放置已久的过氧化钠的成份进行探究,请回答下列问题:
(1)反应 2Na2O2+2H2O=4NaOH+O2↑的还原剂是????????(写化学式);
反应2Na2O2+2CO2=2Na2CO3+O2↑中,每生成1molO2则转移了?????mol电子。
(2)进行探究:
①提出假设。假设1:全部是Na2O2????????假设2:全部是Na2CO3
假设3:???????????????????????
②设计方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂和仪器:蒸馏水、1moL L-1H2SO4、澄清石灰水、淀粉-KI溶液、酚酞溶液、火柴、试管、小烧杯。
L-1H2SO4、澄清石灰水、淀粉-KI溶液、酚酞溶液、火柴、试管、小烧杯。
实验步骤
| 预期现象和结论
|
步骤1:取少量固体样品于试管中,滴加足量1moL L-1 H2SO4至固体溶解,然后将内壁附有澄清石灰水的烧杯罩于试管口。 L-1 H2SO4至固体溶解,然后将内壁附有澄清石灰水的烧杯罩于试管口。
| 若澄清石灰水未见浑浊,则假设1成立;
若澄清石灰水变浑浊,则??????????????
????????????????????????????????????
|
步骤2:
| ?
|
步骤3:
| ?
2、实验题 过氧化钠(Na2O2)是中学常见物质。已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,能被过氧化钠氧化生成硫酸钠,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。
实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:假设1:反应后固体中只有________,证明SO2未被氧化;
假设2:反应后固体中只有________,证明SO2完全被氧化;
假设3:__________________________证明______________________。
实验探究:实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:
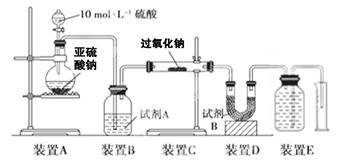
(2)试剂A可以选用________,试剂B的作用是________。
(3)实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下),用上述有关测量数据判断, SO2未被氧化时、完全被氧化的V-m1关系式。
未被氧化:____________,完全被氧化:____________。
(4)若SO2完全被氧化,写出反应的化学方程式: __________________________。
3、选择题 下列说法正确的是(?)
A.Na2CO3比NaHCO3的溶解度小
B.质量相同的Na2CO3和NaHCO3与足量盐酸反应可生成等量的CO2
C.石灰水可鉴别Na2CO3和NaHCO3溶液
D.Na2CO3和NaHCO3同时与质量分数相等.质量相等的盐酸反应,后者放出气体快
4、选择题 将物质的量均为a mol的钠和铝一同投入m g水中(水足量),所得溶液的密度为ρg・Cm-3,则此溶液的物质的量浓度为(??)
A.mol/L
B.mol/L
C.mol/L
D.mol/L
5、计算题 agNa2CO3和NaHCO3混合物加热至质量减少到bg,则混合物 中NaHCO3的质量分数为:????。 中NaHCO3的质量分数为:????。
|