?
�ο��𰸣���16�֣���1����4�֣�Na2O2???? 2
��2��
�����������1����Ӧ�еĵ���ת��Ϊ��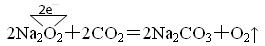 ����Na2O2����������������ԭ��Ӧ���������������ǻ�ԭ����ÿ����ÿ����1molO2��ת����2mol���� ����Na2O2����������������ԭ��Ӧ���������������ǻ�ԭ����ÿ����ÿ����1molO2��ת����2mol����
��2����Na2O2�ڿ�������Ҫ�ǿ��Ժ�CO2��H2O��Ӧ�ֱ�����Na2CO3��NaOH������ΪNaOH�ڿ�������CO2��Ӧ����Ҳ����Na2CO3�����Բ�������NaOH��������
�����Ѷȣ�һ��
2��ʵ���� ��������(Na2O2)����ѧ�������ʡ���֪������������CO2��Ӧ���������ɣ�����SO2ͨ��������Ʒ�ĩ��Ҳ���������ɡ��������CO2��SO2��������Ƶķ�Ӧԭ����ͬ����Ҳ�������SO2���н�ǿ�Ļ�ԭ�ԣ��ܱ����������������������ƣ�CO2��ǿ��ԭ�ԣ���Ӧԭ������ͬ���ݴ��������ʵ����������жϡ�
ʵ��һ����һ�����Ĺ������ƹ�����ͨ��������SO2��ȡ��Ӧ��Ĺ������ʵ��̽������֤������������SO2��Ӧ���ص㡣
��1��������裺����1����Ӧ�������ֻ��________��֤��SO2δ��������
����2����Ӧ�������ֻ��________��֤��SO2��ȫ��������
����3��__________________________֤��______________________��
ʵ��̽����ʵ�����ͨ���������������жϷ����Ļ�ѧ��Ӧ��ʵ��װ�����£�
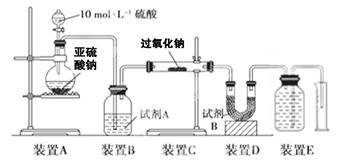
��2���Լ�A����ѡ��________���Լ�B��������________��
��3��ʵ����װ��C�й�����������������m1 g��װ��D����������m2 g��װ��E���ռ���������ΪV L(�ѻ���ɱ�״����)���������йز��������жϣ� SO2δ������ʱ����ȫ��������V-m1��ϵʽ��
δ��������____________����ȫ��������____________��
��4����SO2��ȫ��������д����Ӧ�Ļ�ѧ����ʽ�� __________________________��
�ο��𰸣���1��Na2SO3(1��)???? Na2SO4(1��)??
���������
���������������Ŀ���⣺��1������1����Ӧ�����ֻ�� Na2SO3��֤��SO2δ������������2����Ӧ�������ֻ�� Na2SO4��֤��SO2��ȫ������������3������ΪNa2SO3��Na2SO4�Ļ���֤��SO2���ֱ�������ʵ�������2���������ƺ�ˮ��Ӧ��װ��A���Լ�������ˮ�����������Լ�ΪŨ���ᣬ���������ȥˮ������װ��BΪ�ⶨ�����������������Ҫ��ʣ��Ķ��������ȥ������Լ�Bװ������������δ��Ӧ��SO2����3��ʵ����װ��C�й�����������������m1 g��װ��D����������m2 g��װ��E���ռ���
�����Ѷȣ�һ��
3��ѡ���� ����˵����ȷ���ǣ�?��
A��Na2CO3��NaHCO3���ܽ��С
B��������ͬ��Na2CO3��NaHCO3���������ᷴӦ�����ɵ�����CO2
C��ʯ��ˮ�ɼ���Na2CO3��NaHCO3��Һ
D��Na2CO3��NaHCO3ͬʱ������������ȣ�������ȵ����ᷴӦ�����߷ų������
�ο��𰸣�D
���������
���������A����ͬ���¶��£�̼���Ƶ��ܽ�ȴ���̼�����Ƶģ�A����;Bֱ�����û�ѧ����ʽ���м��㣬����Na2CO3��NaHCO3��������Ϊ1g����
��1��Na2CO3�����������ᷴӦ�����ɵĶ�����̼���������Ϊx��
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106??????????????????? 44
1g????????????????????? x
 �����Ѷȣ�һ�� �����Ѷȣ�һ��
4��ѡ���� �����ʵ�����Ϊa mol���ƺ���һͬͶ��m gˮ��(ˮ����)��������Һ���ܶ�Ϊ��g��Cm-3�������Һ�����ʵ���Ũ��Ϊ��??��
A��mol/L
B��mol/L
C��mol/L
D��mol/L
�ο��𰸣�C
���������
�ƺ���Ͷ������ˮ�з�����Ӧ��2Na+2H2O=2NaOH+H2����2Al+2NaOH+2H2O=2NaAlO2+3H2����
�ɷ���ʽ��֪��a mol���Ʒ�Ӧ����amol�������ƣ���������0.5amol��amol����������amol��ǡ�÷�Ӧ����amolƫ�����ƣ�ͬʱ��������1.5amol����ҺΪƫ��������Һ��
������������0.5amol+1.5amol����2g��mol��1=4ag��
��Һ����m����Һ��=m��������+m��H2O��-m��H2��=amol��23g��mol��1+amol��
�����Ѷȣ�һ��
5�������� agNa2CO3��NaHCO3�������� ���������ٵ�bg�������� ��NaHCO3����������Ϊ��????�� ��NaHCO3����������Ϊ��????��
�ο��𰸣� ����������⣺��NaHCO3������Ϊx ����������⣺��NaHCO3������Ϊx
2NaHCO3====Na2CO3��H2��CO2��????????????????? ��m
168g??????? 106g?????????????????????? 168g��106g��62g
x??????????????????????????????????????��a-b��g
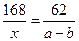 �����Ѷȣ��� �����Ѷȣ���
|