��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����±��ṩ��������ҩƷ�����ܴﵽ��Ӧʵ��Ŀ�ĵ��ǡ�
���
| ����
| ҩƷ
| ʵ��Ŀ��
|
A
| ������ƽ�������룩����ͷ�ιܡ���Ͳ���ձ���ҩ�ס�������
| NaCl���塢����ˮ
| ����һ������������NaCl��Һ
|
B
| ��Һ©������ƿ����ƿ�����ܼ���Ƥ��
| ���ᡢ����ʯ��̼������Һ
| ֤���ǽ����ԣ�Cl>C>Si
|
C
| ��ʽ�ζ��ܡ���ͷ�ιܡ�����̨�������У�
| ��֪Ũ�ȵ����ᡢ����NaOH��Һ
| �ⶨNaOH��Һ�����ʵ���Ũ��
|
D
| �ձ�����Һ©������ͷ�ιܡ�����̨
| ���ᴿ��AlCl3��Һ��NaoH��Һ
| �ᴿ����MgCl2���ʵ�AlCl3��Һ
�ο��𰸣�A
���������
���������A��ҩ������ȡ�ù��壬������ƽ���������������ձ������ܽ���壬��Ͳ��ȡˮ����������������ڽ��裬��������һ��������������Һ����ȷ��B����ʵ�����֤��������̼�����Ե�ǿ��������֤���ǽ����Ե�ǿ��������C��ȱ��ָʾ������ƿ����ʽ�ζ��ܣ��������ζ�ʵ�飬����D��ȱ����ͨ©������ֽ�����ܹ��ˣ�����ѡA��
�����Ѷȣ�һ��
2��ѡ���� ���и���ʵ��������������ó��Ľ�����ȷ���ǣ�????��
ѡ��
| ʵ�����
| ʵ������
| �� ��
| A
| �����ݵ�������Һ�зֱ�μӱ���NaCl��Һ��CuSO4��Һ
| ���������
| �����ʾ���������
| B
| ������ij��ɫ����ͨ�����ʯ��ˮ
| ���ְ�ɫ����
| ������һ����CO2
| C
| �ֱ��òⶨ������0.1 mol��L��-1 Na2SiO3��Na2CO3��PH
| PH:Na2SiO3��Na2CO3
| �ǽ�����Si��C
| D
| ��Ũ�Ⱦ�Ϊ0.1 mol��L��1NaCl��NaI�����Һ�У�
�μ�����AgNO3��Һ
| ���ֻ�ɫ����
| Ksp(AgCl)��Ksp(AgI)
?
�ο��𰸣�D
���������
���������A��ǰ��Ϊ����������Ϊ���ԣ�B���п���ΪSO2���壻C���ܵó�̼������Աȹ�������ǿ����ǽ�����C>Si
����������ʵ������������ƶϻ�ѧ���ʣ��ѶȽϴ��漰��������Ӧ�ķ�Ӧ������Ҫģ��ʵ�飬���ʵ�����飬����ʵ������
�����Ѷȣ���
3��ѡ���� ���л�ѧʵ���ܴﵽĿ�ĵ���
A���ü���ʼ���ijKI��Һ���Ƿ����е���
B������������ˮ����ˣ��ɳ�ȥ���е���������
C�����ˮ�м��뱽��ƾ������ɴӵ�ˮ����ȡ��
D����AgCl�����еμ�����KI��Һ����˵��Ksp(AgCl)��Ksp (AgI)
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
4��ʵ���� Fenton�������ڴ������ѽ����л���Ĺ�ҵ��ˮ��ͨ�����ڵ��ں�pH��Fe2+Ũ�ȵķ�ˮ�м���H2O2�����������ǻ����ɻ�������������Ⱦ������ø÷��������л���Ⱦ��p-CP��̽���й����ضԸý��ⷴӦ���ʵ�Ӱ�졣
[ʵ�����]����p-CP�ij�ʼŨ����ͬ���㶨ʵ���¶���298K��313K������ʵ���������±�����������¶Ա����顣
��1���������ʵ����Ʊ������в�Ҫ���ո�

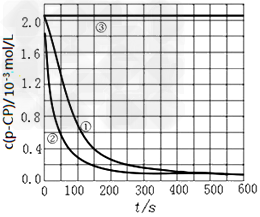
[���ݴ���]ʵ����p��CP��Ũ����ʱ��仯�Ĺ�ϵ��ͼ���٢ڢ۷ֱ������������ʵ���õ��������ߡ�
��2�������ʵ������ߣ����㽵�ⷴӦ�� 50~150s�ڵ�ƽ����Ӧ���ʣ�v(p��CP)=?
_________?mol L-1 L-1 s-1�� s-1��
��3��ʵ��١��ڱ����¶����ߣ��ý��ⷴӦ����_____��?(������С)���������ױ������¶ȹ���ʱ����ӽ�100�棩�������½��ⷴӦ���ʼ�С�����Fenton�������Լ�H2O2�ĽǶȷ���ԭ��?_________________________________��
��4��ʵ��۵ó��Ľ����ǣ�pH����10ʱ��_________________________
��5��ʵ��ʱ���ڲ�ͬʱ��ӷ�Ӧ����ȡ������ʹ��ȡ��Ʒ�з�Ӧ����ֹͣ������������ͼ�е���Ϣ������һ��Ѹ��ֹͣ��Ӧ�ķ�����_____________________________��
�ο��𰸣���1��![]() ��������� ���������
�����Ѷȣ�һ��
5��ʵ���� ��Уij��ѧС�������ʵ�����ŨH2SO4��ľ̿��Ӧ�����в���:
(1)д��ŨH2SO4��ľ̿��Ӧ�Ļ�ѧ����ʽ_____________
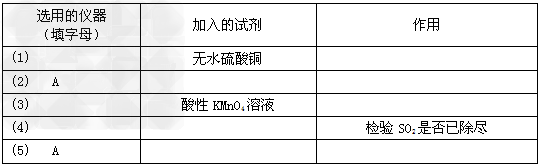
(2)�������ͼ��ѡ����������������ظ�ʹ�ã����һ��װ�ð�����С��ʵ�����ǵ�Ŀ��.���ṩŨH2SO4��ľ̿������KMnO4��Һ����ˮ����ͭ�������̡�Һ�Լ���ѡ�������Ӻ̶������õIJ����ܡ����ܡ����С�����̨������װ�õȾ���ȥ��??
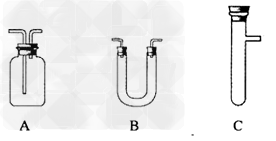
����ѡ������������˳�������������������±�(���Բ�����,Ҳ���Բ���)����д����������Ӧ���Լ������Ƽ������á�
�ο��𰸣���1��2?H2SO4?(Ũ)?+?C![]() ��������� ���������
�����Ѷȣ�һ��
|
|