微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 SO2通入足量Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。针对上述一系列变化过程中,下列说法中不正确的是
A.上述过程中,最终被还原的是NO3--
B.从上述过程中可以得出结论,氧化性:HNO3>Fe3+>稀H2SO4
C.上述过程中,会产生一种无色无味的难溶于水的气体
D.假设通入的SO2完全反应,则同温同压下,S O2和逸出气体的体积为1∶1
O2和逸出气体的体积为1∶1
参考答案:D
本题解析:略
本题难度:一般
2、选择题 下列叙述中,正确的是( )
A.浓硫酸能将炽热的木炭氧化为二氧化碳
B.稀硫酸能按水的组成比脱去蔗糖中的氢、氧元素
C.硫酸和硝酸分别与金属反应时,S和N元素的化合价一定发生变化
D.因为浓硫酸或浓硝酸能与铝反应,所以常温下二者都不能用铝制容器盛装
参考答案:A
本题解析:
试题分析:浓硫酸能将炽热的木炭氧化为二氧化碳,故A正确;B错误,应该是浓硫酸能按水的组成比脱去蔗糖中的氢、氧元素,;C错误,稀硫酸与金属反应时,S元素的化合价不发生变化;D错误,虽然浓硫酸或浓硝酸能与铝反应,但是反应生成了致密的氧化物薄膜,可以阻止反应的进行,所以在常温下可以用铝制容器盛装浓硫酸或浓硝酸。
点评:本题考查了化学基本概念,属于对基础知识的考查,该题有利于考查学生对化学基本概念的掌握情况,本题比较容易。
本题难度:一般
3、实验题 浓硫酸有强氧化性,铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。请你协助他们探究所得气体的成分。
Ⅰ【提出猜想】
猜想1:所得气体中可能是SO2。 ????猜想2:所得气体中可能是__________。
猜想3:所得气体中可能是_______的混合气体。
Ⅱ【实验探究】
(1)将所得气体通入如下装置
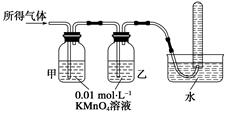
证明猜想3正确的实验现象是___________、______________、________________。
(2)点燃余下的气体前,必须要进行的操作是_________________________________。
(3)写出浓硫酸表现出强氧化性的化学反应方程式_____________________________。
(4)如果把一定量的铁与浓硫酸加热时产生的气体通过装有过量Na2O2粉末的玻璃管,则玻璃管中反应的生成物可能含有(填化学式)__________________ ___________ _。
参考答案:Ⅰ猜想2:H2????猜想3:SO2和H2
Ⅱ(1)
本题解析:
试题分析:Ⅰ:铁是比较活泼的金属。比较活泼的金属与酸反应置换出氢气。所以猜想2的气体可能是H2。浓硫酸是氧化性的酸,反应开始时首先是浓硫酸与铁发生氧化还原反应2Fe+6H2SO4(浓) Fe2(SO4)3+3SO2↑+6H2O。随着反应的进行,硫酸变为稀硫酸这时发生反应:Fe+H2SO4(稀)=FeSO4
Fe2(SO4)3+3SO2↑+6H2O。随着反应的进行,硫酸变为稀硫酸这时发生反应:Fe+H2SO4(稀)=FeSO4
本题难度:一般
4、选择题 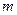 g铜与足量浓H2SO4共热时恰好完全反应,在标准状况下生成
g铜与足量浓H2SO4共热时恰好完全反应,在标准状况下生成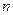 L气体,则被还原的H2SO4的量是
L气体,则被还原的H2SO4的量是
A.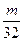 mol
mol
B.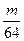 mol
mol
C.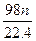 g
g
D.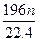 g
g
参考答案:BC
本题解析:略
本题难度:一般
5、选择题 下列物质中,能使品红溶液褪色的是
A.甲烷
B.盐酸
C.二氧化硫
D.二氧化碳
参考答案:C
本题解析:
试题分析:在所给的物质中,只有SO2具有漂白性,能使品红溶液褪色,其余选项不可以,因此正确的答案选C。2的漂白性
点评:该题是基础性试题的考查,主要是对教材基础知识的巩固和训练。该题是识记性知识的检验,难度不大,记住常见的漂白剂以及漂白原理即可。
本题难度:简单