微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有K2SO4和Fe2(SO4)3的混合溶液,含Fe3+的物质的量浓度为0.1mol/L,而SO42-的物质的量浓度为0.3mol/L,则混合溶液中K+的物质的量浓度为
A.0.15mol/L
B.0.3mol/L
C.0.45mol/L
D.0.6mol/L
参考答案:B
本题解析:分析:根据电荷守恒有3c(Fe3+)+c(K+)=2c(SO42-),据此计算.
解答:K2SO4和Fe2(SO4)3的混合溶液,含Fe3+的物质的量浓度为0.1mol/L,SO42-的物质的量浓度为0.3mol/L,
根据电荷守恒有3c(Fe3+)+c(K+)=2c(SO42-),
即3×0.1mol/L+c((K+)=2×0.3mol/L,
解得c(K+)=0.3mol/L,
故选B.
点评:本题考查离子浓度的有关计算,难度不大,注意电解质混合溶液中离子浓度计算中电荷守恒思想的利用.
本题难度:困难
2、选择题 把Cl2通入下列溶液中,阴阳离子均被氧化的是
A.NaI
B.AgF
C.FeCl2
D.FeBr2
参考答案:D
本题解析:分析:氯气具有强氧化性,把Cl2通入下列溶液中,阴阳离子均被氧化,说明物质所含的阴阳离子均具有还原性,都可被氯气氧化,以此解答该题.
解答:A.钠离子不能被氧化,故A错误;
B.银离子和氟离子都不能被氧化,故B错误;
C.氯离子不能被氧化,故C错误;
D.亚铁离子和溴离子都能被氧化,故D正确.
故选D.
点评:本题考查氯气的性质,题目难度不大,注意把握氯气的氧化性以及物质的氧化性强弱的比较.
本题难度:困难
3、选择题 在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是
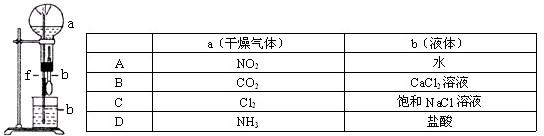
A.A
B.B
C.C
D.D
参考答案:D
本题解析:分析:此题要从反应物和生成物的状态变化入手,注意到反应后气体减少或增多会引起气压的变化,将化学和物理结合起来,气体被吸收进溶液的反应,容器内气体减少,气压减小;容器内气体增多,气压增大;
解答:A、NO2与水反应,生成硝酸和NO,容器内气体减少,气压减小,形成喷泉,但由于NO不溶于水,所以不充满烧瓶.故A错误;
B、CO2与CaCl2溶液不反应,锥形瓶与烧瓶内压强相等,不能形成喷泉,故B错误;
C、Cl2不溶于饱和氯化钠溶液,也不与其反应,锥形瓶与烧瓶内压强相等,不能形成喷泉,故C错误;
D、NH3与盐酸能发生反应,生成物为氯化铵固体,气体被吸收进溶液中,烧瓶内压强减小为零,同外界大气压产生压强差,所以形成喷泉,并充满烧瓶,故D正确;
故选D.
点评:从此题实验来看,反应物或生成物的状态变化会引起气压的变化,说明化学不是一门单独存在的学科,化学和物理是相互联系的,解决化学问题可以应用物理知识.
本题难度:困难
4、选择题 在一定温度和压强下,1体积的A2气体和3体积B2气体化合成2体积的C气体,则C的化学式为
A.AB3
B.AB
C.A3B ? ? ? ? ? ??
D.A2B3
参考 答案:A
本题解析:由阿伏加德罗定律可知此反应的化学方程式为A2+3B2=2C,设C的化学式为AmBn,由质量守恒定律得:
A原子守恒:1×2=2m
B原子守恒:3×2=2n
可求
所以,C的化学式为AB3。
本题难度:一般
5、选择题 当铁与硫的混合物29 g在密闭条件下加热反应后,冷却至室温,再与足量稀H2SO4反应,得到气体8.4 L(标准状况下),则原混和气体中铁与硫的物质的量之比为
A.1∶1
B.1∶2
C.2∶3
D.3∶2
参考答案:D
本题解析:
本题难度:简单