微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 称取两份铝粉,第一份加入足量的浓NaOH(aq),第二份加入足量的HCl(aq),如果放出的气体体积为1:3(在同温同压下),则两份铝粉的质量之比为
A.1:2
B.1:3
C.3:2
D.1:1
参考答案:B
本题解析:分析:因酸、碱足量,则铝完全反应,由电子守恒来计算Al的物质的量,铝的物质的量之比等于质量之比.
解答:放出的气体体积为1:3,设生成的氢气的物质的量分别为1mol、3mol,
设第一份中的Al的物质的量为x,第二份中的Al的物质的量为y,
因酸、碱足量,则铝完全反应,
由电子守恒可知,
x×3=1mol×2×(1-0),
y×3=3mol×2×(1-0),
解得x=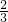 mol,y=2mol,
mol,y=2mol,
则两份铝粉的质量之比为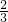 mol:2mol=1:3,
mol:2mol=1:3,
故选B.
点评:本题考查铝与酸、碱的反应,明确酸碱足量及反应均为氧化还原反应,利用电子守恒来计算是解答的关键.
本题难度:困难
2、选择题 在加入Al能产生H2的溶液中一定能存在的离子是
A.HCO3-
B.CO32-
C.Na+
D.Mg2+
参考答案:C
本题解析:分析:在加入Al能产生H2的溶液,可能为酸或碱的溶液,则与氢离子或氢氧根离子反应的离子,一定不能存在,以此来解答.
解答:在加入Al能产生H2的溶液,可能为酸或碱的溶液,
A.HCO3-既能与酸反应又能与碱反应,则一定不存在,故A不选;
B.CO32-能与酸反应生成水和气体,则一定不存在,故B不选;
C.Na+既不能与酸反应又不能与碱反应,则一定存在,故C选;
D.Mg2+能与碱反应生成沉淀,则一定不存在,故D不选;
故选C.
点评:本题考查离子的共存问题,明确信息是解答本题的关键,并利用离子之间的反应来解答,难度不大.
本题难度:一般
3、选择题 为了验证碳酸氢钠固体中是否含有碳酸钠.下列实验及判断中,正确的是
A.加热,观察是否有气体放出
B.溶于水后加石灰水,看有无沉淀
C.取少量配成稀溶液滴加氯化钡溶液,看有无沉淀
D.加热后称量,看质量是否变化
参考答案:C
本题解析:分析:A、碳酸钠受热稳定,碳酸氢钠受热分解为碳酸钠、水、二氧化碳;
B、碳酸钠和碳酸氢钠均可以和石灰水反应产生白色沉淀碳酸钙;
C、碳酸钠可以和氯化钡发生复分解反应但是碳酸氢钠不能反应;
D、碳酸氢钠加热后分解,碳酸钠加热后不变.
解答:A、碳酸氢钠固体中不管是否含有碳酸钠,加热后均会产生气体,故A错误;
B、碳酸钠和碳酸氢钠均可以和石灰水反应产生白色沉淀碳酸钙,故B错误;
C、碳酸钠可以和氯化钡发生复分解反应生成白色沉淀碳酸钙,但是碳酸氢钠不能反应,故C正确;
D、碳酸氢钠本身加热后称量质量会减轻,碳酸氢钠固体中否含有碳酸钠加热后称量质量仍然会减轻,故D错误.
故选C.
点评:本题考查学生碳酸钠和碳酸氢钠的化学性质,可以根据所学知识进行回答,难度不大.
本题难度:困难
4、选择题 下列物质是不属于电解质的是
A.CO2
B.(NH4)2SO4
C.Cl2
D.BaSO4
参考答案:AC
本题解析:单质既不是电解质也不是非电解质。CO2是非电解质,(NH4)2SO4、BaSO4
是电解质。
本题难度:简单
5、选择题 常温下在稀盐酸中插入一小块铜片,加入下列物质后,可使铜片溶解的是
A.浓硝酸
B.硫酸钠晶体
C.硝酸钾晶体
D.氯化铁晶体
参考答案:ACD
本题解析:由下面方程式可知:
3Cu+8H++2NO3-=2Cu2++2NO↑+4H2O??? Cu+2Fe3+=2Fe2++Cu2+
向盐酸中加入硝酸或硝酸盐或铁盐,均可使铜溶解,故答案为ACD
本题难度:简单