微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 可以用来鉴别0.1mol/L的Na2S、NaI、Na2CO3、NaAlO2、Na2SO4五种溶液的是
A.烧碱溶液
B.氯化钡溶液
C.氨水
D.硫酸铁溶液
参考答案:D
本题解析:分析:依据Na2S、NaI、Na2CO3、NaAlO2、Na2SO4五种溶液中的阴离子的性质不同选择合适的检验物质,反应时分别出现不同的现象既可以一次性检验;检验S2-、AlO2-、CO32-可用H+,也可以用三价铁盐根据反应现象不同检验,检验I-可用氧化剂把碘离子氧化为碘单质,利用溶液颜色的变化进行鉴别,检验硫酸钠是加入盐酸再加入氯化钡,有白色沉淀说明含硫酸根离子;
解答:A、加入NaOH溶液,与Na2S、NaI、Na2CO3、NaAlO2、Na2SO4都不反应,无法鉴别,故A错误;
B.加入BaCl2溶液,Na2CO3、和Na2SO4都生成白色沉淀,不能鉴别,故B错误;
C.加入氨水,与Na2S、Na2CO3、Na2A1O2、Na2SO4都不反应,不能鉴别,故C错误;
D.加入硫酸铁,与Na2S反应生成红褐色沉淀和臭鸡蛋气味的气体、与NaI反应溶液无色变为紫色、与Na2CO3反应生成红褐色沉淀和无色无味的气体、与NaAlO2反应生成红褐色沉淀和白色、与Na2SO4不反应;故正确;
故选D.
点评:本题考查了几种阴离子的鉴别方法,关键是各离子的性质特征.
本题难度:一般
2、选择题 下列试剂中,能将NaCl、NH4Cl和FeCl3三种溶液区分开的是
A.HNO3溶液
B.BaCl2溶液
C.NaOH溶液
D.AgNO3溶液
参考答案:C
本题解析:分析:NaCl、NH4Cl和FeCl3三种溶液分别与NaOH溶液反应的现象为:无现象、有刺激性气味的气体、红褐色沉淀,现象不同,以此来解答.
解答:A.HNO3溶液与三者溶液均不反应,不能区分,故A错误;
B.BaCl2溶液与三者溶液均不反应,不能区分,故B错误;
C.NaCl、NH4Cl和FeCl3三种溶液分别与NaOH溶液反应的现象为:无现象、有刺激性气味的气体、红褐色沉淀,现象不同,能区分,故C正确;
D.AgNO3溶液与三者溶液反应均生成白色沉淀,现象相同,不能区分,故D错误;
故选C.
点评:本题考查物质的区分,明确物质的性质及发生的化学反应是解答本题的关键,侧重物质性质的考查,题目难度不大.
本题难度:简单
3、选择题 用一种试剂就能鉴别NaHCO3、BaCl2、KNO3三种物质,此试剂是
A.盐酸
B.Ba(OH)2溶液
C.硫酸
D.BaCl2溶液、加热
参考答案:C
本题解析:分析:进行物质鉴别时,要根据物质的性质差异进行,所选的鉴别试剂与物质混合时要有明显的不同现象.
解答:A、盐酸和氯化钡以及硝酸钾均不反应,二者无法鉴别,故A错误;
B、氢氧化钡和氯化钡以及硝酸钾均不反应,二者无法鉴别,故B错误;
C、稀硫酸与氯化钡混合能产生白色沉淀,而硝酸钾混合时无现象,和碳酸氢钠反应会生成二氧化碳气体,现象不一样,可以鉴别,故B正确;
D、氯化钡和氯化钡溶液以及硝酸钾混合均不反应,无现象,二者无法鉴别,故D错误.
故选C.
点评:本题考查了常见物质的鉴别,完成此题,可以依据物质的性质进行,所选的鉴别试剂与待鉴别物质混合时要有明显的不同现象.
本题难度:简单
4、选择题 下列各组物质的无色溶液,不用其它试剂即可鉴别的是
①KOH、Na2SO4、AlCl3??????????
②NaAlO2、HCl、H2SO4
③Na2CO3、NaHCO3、H2SO4
④AgNO3、Na2CO3、KCl.
A.①②④
B.②③
C.①②
D.①③
参考答案:D
本题解析:分析:根据物质的性质及相互反应的现象进行分析,解答此类题一般先看颜色、闻气味、进行焰色反应,再相互反应或利用两种物质相互反滴,让已被检出的物质作已知物再去鉴别其它物质.
解答:①先两两反应,其中一种物质与另外两种物质无明显现象,该物质是Na2SO4,将剩余的两种物质进行滴加反应,KOH滴加到AlCl3中先出现白色沉淀,后白色沉淀溶解,若将加入AlCl3滴加到KOH中先不出现白色沉淀,后出现白色沉淀,据此可以鉴别KOH与AlCl3,故①正确;
②先两两反应,其中一种物质与另外两种物质反应都有沉淀产生,该物质是NaAlO2,但HCl、H2SO4 不能鉴别开,故②错误;
③先两两反应,其中一种物质与另外两种物质反应都有气体生成,则该物质是H2SO4,H2SO4滴加到Na2CO3中,先不产生气体,后产生气体,H2SO4滴加到NaHCO3中立即产生气体,据此可以鉴别Na2CO3、NaHCO3,故③正确;
④先两两反应,其中一种物质与另外两种物质反应都有白色沉淀生成,则该物质是AgNO3,Na2CO3、KCl不能鉴别开,故④错误;
故选D.
点评:不同考查物质检验与推断、元素化合物知识、学生综合分析能力,难度中等,掌握化合物的基础知识与相应的现象是解题的关键,注意不用试剂进行的鉴别一般先看颜色(对气体可以闻气味)、进行焰色反应,再相互反应或利用两种物质相互反滴,让已被检出的物质作已知物再去鉴别其它物质.
本题难度:简单
5、选择题 某同学为检验某溶液中是否含有常见的四种离子,实验操作及现象如图所示:
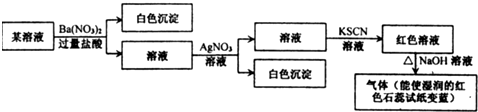
由该实验可知原溶液中一定含的离子是
A.SO42-
B.NH4+
C.Cl-
D.Fe3+
参考答案:B
本题解析:分析:在溶液中加入盐酸酸化的硝酸钡,其中的亚硫酸根离子、亚铁离子会被氧化为硫酸根离子、铁离子,加入的盐酸中含有氯离子,会和硝酸银反应生成氯化银白色沉淀,能使红色石蕊试纸变蓝的气体是氨气,三价铁离子能使硫氰酸钾变为红色.
解答:A、原溶液中加入盐酸酸化的硝酸钡,如果其中含有亚硫酸根离子,则会被演化为硫酸根离子,所以原溶液中不一定含有SO42-离子,故A错误;
B、产生能使红色石蕊试纸变蓝的气体是氨气,所以原来溶液中一定含有铵根离子,故B正确;
C、原溶液中加入盐酸酸化的硝酸钡,引进了氯离子,能和硝酸银反应生成氯化银沉淀的离子不一定是原溶液中含有的氯离子,可能是加进去的盐酸中的,故C错误;
D、原溶液中加入盐酸酸化的硝酸钡,如果其中含有亚铁离子,则亚铁离子会被氧化为铁离子,铁离子能使硫氰酸钾变为红色,所以原溶液中不一定含有Fe3+离子,故D错误.
故选B.
点评:本题是一道关于离子反应和离子检验知识的题目,考查学生分析和解决问题的能力,难度中等.
本题难度:一般