��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �����£����и���������ָ����Һ�п��ܴ����������
A���ڼ�����Һ�У�K+��Cl-��Na+��CO32-
B����c(H+)/ c(OH-)=1��10-12����Һ�У�Ca2+��Cl?-��K+��NH4+
C����������Һ�У�Cu2+��Fe3+��I-��SO42-
D�������۷�Ӧ�ų���������ɫ��Һ�У�K+��NO3-��Cl-��HCO3-
�ο��𰸣� A
���������
���������A���ڼ�����Һ�У�K+��Cl-��Na+��CO32-�����Դ������棬A��ȷ��B����c(H+)/ c(OH-)��1��10-12����Һ�и���ˮ�����ӻ�������֪����Һ����c(H+)��1��10-13mol/L������Һ�Լ��ԣ����Ca2+��NH4+���ܴ������棬B����ȷ��C��Cu2+��Fe3+��I-������������ԭ��Ӧ�����ܴ������棬C����ȷ��D�������۷�Ӧ�ų���������ɫ��Һ���������ԣ�Ҳ�����Լ��ԣ�����Լ��ԣ�HCO3-���ܴ������棬���������HCO3-Ҳ���ܴ������棬����������Һ��NO3-������Ӧ
�����Ѷȣ�һ��
2��ѡ���� �����£����и���������ָ����Һ��һ���ܴ����������
A��ʹ���ȳʺ�ɫ����Һ�У�K+��AlO2����NO3����CO32��
B��c(ClO��)��1.0 mol��L��1��Һ��Na+��SO32����S2����Cl��
C��ˮ���������c(H+)=1��10-12����Һ��K����NH4+��SO42����Fe3+
D��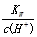 ��0.1 mol��L��1����Һ��Na����AlO2����CO32-��NO3��
��0.1 mol��L��1����Һ��Na����AlO2����CO32-��NO3��
�ο��𰸣�D
���������
���������A��ʹ���ȳʺ�ɫ����ҺΪǿ������Һ������������AlO2����CO32�������������������Һ�У���A�����B��ClO��Ϊǿ���������ӣ��ܽ�SO32����S2���������ʲ��ɴ�����������Һ�У���B�����C��ˮ���������c(H+)=1��10-12����Һ����Һ��ˮ�������c(H+)=1��10-12���ʸ���Һ������ˮ�ĵ��룬�����ҺΪ���������ҺΪ��ʱ�������Ӳ�������ѧ��Ӧ���ʿɴ�����������Һ�У�������ҺΪ��ʱ��NH4+��Fe3+��OH�����������������Һ�У���C�����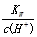 ��0.1 mol��L��1����ҺΪ������Һ���ڼ�����Һ��Na����AlO2����CO32-��NO3����������ѧ��Ӧ���ʿɴ�����������Һ�У���D����ȷ������ѡD��
��0.1 mol��L��1����ҺΪ������Һ���ڼ�����Һ��Na����AlO2����CO32-��NO3����������ѧ��Ӧ���ʿɴ�����������Һ�У���D����ȷ������ѡD��
���㣺���Ӵ����������⡣
�����Ѷȣ�����
3��ѡ���� ���и�����������ˮ�ⷴӦ�����ܴ����������
A��Ba2+��Cl����Na+��SO42��
B��AlO2����K+��HCO3����Cl��
C��OH����Fe3+��NO3����SO42��
D��Al3+��Na+��HCO3����Cl��
�ο��𰸣�D
���������
���������A��Ba2+��SO42�������ɳ������ܴ������棬B��AlO2����HCO3����Ϊ����ǿ�������ᷴӦ���ܴ������棬C��OH����Fe3+��Ϊ���ɳ������ܴ������棬D��Al3+��HCO3����Ϊ����˫ˮ�ⷴӦ���ܴ������档��ѡD��
���������Ӳ��ܴ��������һ������ǣ���1���ܷ������ֽⷴӦ������֮�䣨�����ɳ��������壬ˮ�����ᡢ������ѵ������ʣ�����2�������������������֮�䣨�磺Ca2+�� SO42-��Ag+�� SO42-������3������ȫˮ�������֮�䣬���Ԫ����������ε����������ӣ���
�����Ѷȣ�һ��
4��ѡ���� ������Һ�У�����Ũ�ȹ�ϵ��ȷ����
A��0.1mol��L-1 pHΪ4��NaHSO3��Һ�У�c(HSO3�D) > c(SO32�D)> c(H2SO3)
B������������ʵ���Ũ��NaF ��Һ��HF��ϣ�c(Na��)=c(F�D)+c(HF)
C����NaHA��Һ��һ���У�c(Na��)+c(H��) = c(HA�D)+c(OH�D)+c(A2-)
D��c(NH4��)���Ũ�ȵ�(NH4)2CO3��(NH4)2SO4��(NH4)2Fe(SO4)2������Һ���ʵ���Ũ����������
�ο��𰸣�A
���������A��HSO3���ĵ���̶ȴ���ˮ��̶ȣ���A��ȷ
B��F����H2O HF��OH�D��HF
HF��OH�D��HF H����F���������2c(
H����F���������2c(
�����Ѷȣ�һ��
5��ѡ���� ����ڴ���Na+��Cl-����Һ��ͨ��������NH3����Һ�л����ܴ������ڵ���������[???? ]
A��K+��Br-��CO32-
B��Al3+��H+��MnO4-
C��NH4+��Fe3+��SO42-
D��Ag+��Cu2+��NO3-
�ο��𰸣�A
���������
�����Ѷȣ�һ��