��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� V?L��������Һ�к�Al3+������Ϊm?g������Һ��SO42-�����ʵ���Ũ��Ϊ
A.mol?L-1
B.mol?L-1
C.mol?L-1
D.mol?L-1
�ο��𰸣�B
����������������������Ļ�ѧʽΪAl2��SO4��3����n= �ȼ���Al3+�����ʵ������ɻ�ѧʽ�����ӵĹ�ϵ��ȷ��SO42-�����ʵ�����Ȼ������c=
�ȼ���Al3+�����ʵ������ɻ�ѧʽ�����ӵĹ�ϵ��ȷ��SO42-�����ʵ�����Ȼ������c= ������SO42-�����ʵ���Ũ�ȣ�
������SO42-�����ʵ���Ũ�ȣ�
���Al3+�����ʵ���Ϊ =
= mol��
mol��
���������Ļ�ѧʽΪAl2��SO4��3��
��SO42-�����ʵ���Ϊ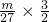 mol=
mol=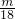 mol��
mol��
����Һ��SO42-�����ʵ���Ũ��Ϊ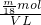 =
=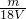 mol?L-1��
mol?L-1��
��ѡB��
���������⿼�����ʵ���Ũ�ȵļ��㣬��ȷ���ʵ����������Ũ�ȵĹ�ϵ���ɽ�𣬱�����ѵ������������ӵ��������������ӵ����ʵ����������ӵ��������Բ������������
�����Ѷȣ�һ��
2������� ��1���·���մ�ж���ֲ�����ۣ���ˮϴ����������������ϴȥ��������Ϊ������л�����______����______���л������������Ͻ����֣�������Ϊ��������л���______��
��2��Ϊ�˼���ͳ�ȥ�±��еĸ��������е����ʣ�����������ʣ�����ӣ� I����ѡ���ʵ��ļ����Լ����ӣ� II����ѡ���ʵ��ij����Լ�������ѡ�Ĵ�������Ӧ�Ŀո��ڣ�
�� I��������Լ���A����ˮ����ͭB�����Ը��������ҺC������D������������Һ
�� II�������Լ���a������??b�����Ը��������Һ??c�����Ƶ���ʯ��d����ˮ
| ���� | �����Լ� | �����Լ�
���飨��ϩ��
�ƾ���ˮ��
�ο��𰸣���1��������л���������ˮ���������л��ܼ�������ֲ����������
���������
�����Ѷȣ���
3��ѡ���� �������ʵļ�������ȷ����(����)
A������ɫ��Ӧ����NaCl��KCl��K2SO4
B��������������Һ����MgCl2��Һ��AlCl3��Һ
C�����ö����ЧӦ����Fe(OH)3������FeCl3��Һ
D�����Ȼ�����Һ����Na2CO3��NaHCO3������Һ
�ο��𰸣�A
���������
���������A���ɫ��Ӧ������Ԫ�ص��������ʣ����ں��������ʶ���KԪ�أ����������ɫ��Ӧ����������ʴ�����ѡA��
���������������ʵļ�������������Ӧ��֪ʶ������ѧ���Ի���֪ʶ�����ճ̶ȣ���Ŀ���ס�
�����Ѷȣ�һ��
4��ѡ���� �����漰�л�������ķ����ᴿ��˵����ȷ����
A����ȥ�����л��е���ϩ���ɽ��������ͨ�����Ը��������Һ
B�����顢��ϩ�ͱ��ڹ�ҵ�϶���ͨ��ʯ�ͷ���õ�
C����ȥ�屽�л��е�Br2������NaOH��Һϴ�ӷ�Һ
D�����������е�����������Ҵ���������������Һ��ȥ
�ο��𰸣�C
���������
���������A����ȷ����Ϊ���Ը��������Һ�ܰ���ϩ��������CO2��Ӧ������ˮ��ʯ�ͷ���ò������顢��ϩ�ͱ���B����ȷ����������������Һ����Ӧ����������ܽ�������������Һ�У�C��ȷ������������ʹ��������ˮ�⣬D����ȷ��Ӧ���ñ���̼������Һ����ѡC��
�������������л��е����ʳ�ȥ����ô�������ᴿ���������һ��IJ�ͬ���ʱ˴˷ֿ����õ���Ӧ��ֵĸ�������з��롣�ڽ�����ʷ����ᴿ����ʱ,ѡ���Լ���ʵ���������Ӧ��ѭ����ԭ��: 1.���������µ����ʣ�ˮ���⣩���������ᴿ�������Ӧ�Ǵ����������Һ�����������������ʻ������У�2.�����ᴿ�������״̬���䣻3.ʵ����̺Ͳ������������У���ѡ������ᴿ����Ӧ��ѭ��������ѧ���ȼ��ӵ�ԭ��
�����Ѷȣ�һ��
5������� ���������û�������������������ų��ķ�������Ҫ��ѧ�ɷ�ΪSiO2Լ45%��Fe2O3Լ40%��Al2O3Լ10%��MgOԼ5%��Ŀǰ�ҹ��Ѿ��ڼ�����ȡ��ͻ�ơ������������з�������ֳɷֲ��������á������̺�����������£�
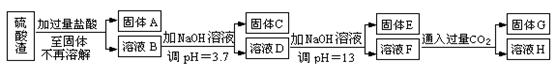
�����ϵ�֪��
��������
| �ܶȻ�(Ksp)
| pHֵ
| ��ʼ����
| ��ȫ����
| Mg(OH)2
| 5.6��10��12
| 9.3
| 10.8
| Fe(OH)3
| 2.8��10��16
| 2.7
| 3.7
| Al(OH)3
| 1.3��10��33
| 3.7
| 4.7
?
��ش��������⣺
��1��д������A�Ļ�ѧʽΪ??????????��
��2����Ҫ�ⶨ��Һ��pH�Ƿ�ﵽ3.7������ʵ����Ʒ�п�ѡ�õ���??????��
A��ʯ����Һ???? B���㷺pH��ֽ??? C������pH��ֽ??? D��pH��
��3������������ӷ�Ӧ����ʽ
����ҺD���ɹ���E?????��??????����ҺF���ɹ���G??????��
��4��Ҫ������C������E����G��ת��Ϊ��Ӧ���ȶ����������е�ʵ�����Ϊ?????��
��5������������Һ����ı仯���������ҺH��c��Mg2����=??????��
�ο��𰸣���1��SiO2��2�֣�
��2��CD��2�֣�
��3
���������
�����������1����һ���мӹ������ᣬFe2O3��Al2O3��MgO�����ᷴӦ�ܽ⣬SiO2���ܹ��˿ɵã���2��A��ֻ���ж���Һ������ԣ�����B���㷺pH��ֽ ֻ�ܾ�ȷ��������������pH��ֽ ��pH�ƶ����ܾ�ȷ��С�����һλ����ࣻ��4�������еõ��Ĺ���Ϊ��������������տɵ������
��5����ҺHΪ����pH=13��õ�����Һ��c(OH��)=0.1 mol/L
c(Mg2+)= Ksp��c2(OH��)= 5.6��10��12��0.12=5.6��10�D10mol/L
�����Ѷȣ�һ��
|
|