微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用NA表示阿伏德罗常数,下列叙述正确的是
A.标准状况下,22.4LH2O含有的分子数为1 NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,1 NA个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1 NA
参考答案:B
本题解析:
正确答案:B
A、不正确,水是液态;C、不正确,应在标准状况下;D、不正确,缺少体积,无法计算。
本题难度:一般
2、选择题 将标准状况下的a升氯化氢气体溶于1000克水中,得到的盐酸的密度为b克/毫升,则该盐酸的物质的量的浓度是
A.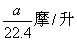
B.
C.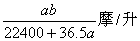
D.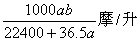
参考答案:D
本题解析:略
本题难度:简单
3、填空题 (1)实验室用氯化铵固体制取氨气的化学方程式是 。
(2)将4.48L(标准状况)氨气通入水中得到0.05L溶液,所得溶液的物质的量浓度是 。
(3)现有100mL AlCl3与MgSO4的混合溶液,分成两等份。
①向其中一份中加入10mL 4mol/L的氨水,恰好完全反应,其中AlCl3与氨水反应的离子方程式是 。继续加入l mol/L NaOH溶液至10mL时,沉淀不再减少,沉淀减少的离子方程式是 ,减少的沉淀的物质的量是 。
②向另一份中加入a mL 1mol/LBaCl2溶液能使SO42-沉淀完全,a= 。
参考答案:(1)Ca(OH)2+2NH4Cl 本题解析:
本题解析:
 试题分析:⑴实验室用氯化铵固体制取氨气的化学方程式是Ca(OH)2+2NH4Cl
试题分析:⑴实验室用氯化铵固体制取氨气的化学方程式是Ca(OH)2+2NH4Cl CaCl2+2H2O+2NH3↑
CaCl2+2H2O+2NH3↑
⑵根据c=n/V,得氨气的物质的量是4.48L/22.4L/mol=0.2mol,所以所得溶液物质的量浓度为:0.2mol/0.05L="4" mol/L
⑶①AlCl3与氨水反应的离子方程式是A13++3NH3・H2O=Al(OH)3↓+3NH4+,沉淀减少即氢氧化铝溶于氢氧化钠溶液,离子方程式为Al(OH)3+OH-=AlO2-+2H2O,沉淀减少的物质的量即为氢氧化钠的物质的量0.01mol
②由①知Al(OH)3的物质的量为0.01mol,消耗NH3・H2O0.03mol,所以Mg2+消耗NH3・H2O(0.04mol-0.03mol)=0.01mol,则n(Mg2+)=0.005mol=n(SO42-),所以需要1mol/LBaCl2溶液5ml使SO42-沉淀完全。
考点:离子反应及相关计算
本题难度:一般
4、选择题 将4gNaOH固体溶于水配成50mL溶液,其物质的量浓度为( )
A.0.1mol/L
B.2mol/L
C.1mol/L
D.0.5mol/L
参考答案:4gNaOH的物质的量=
本题解析:
本题难度:一般
5、选择题 下列各组物质中,所含分子数相同的是( )。
A.10 g H2和10 g O2
B.5.6 L N2(标准状况)和44 g CO2
C.9 g H2O和0.5 mol Br2
D.224 mL H2(标准状况)和0.1 mol N2
参考答案:C
本题解析:由物质的量相关公式可知:A项中两者的摩尔质量不同,等质量时,n不同;B:两者的n分别为0.25mol、1mol,不同;C两者均为0.5 mol;D前者n为0.01 mol,n不同,故为C
本题难度:一般