微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分)同温同压下,等质量的SO2和O2,两者体积比为_________,分子个数比为________,密度比为__________。
参考答案:1:2、 1:2、 2:1(每空2分
本题解析:
试题分析:根据n=m/M得出SO2和O2的物质的量之比为1:2,V=n×Vm,则体积之比等于物质的量之比,所以体积之比为1:2,N=n×NA分子个数之比等于物质的量之比,故为1:2,ρ=m/V,质量相等,密度与体积成反比,为2:1。
考点:有关物质的量的计算。
本题难度:一般
2、选择题 将4.6g钠放入95.4g水中, 所得溶液的质量分数是??(???)
A?等于4.6%??????? B等于8%???????? C? 4.6% ~8%??????? D 大于 8%
参考答案:D
本题解析:正确答案C
由方程式
2Na+2H2O=2NaOH+H2↑
46?? 36??? 40?? 2
4.6g? 3.6g? 4.0g? 0.2g
ω(NaOH)=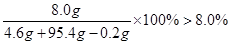
本题难度:一般
3、选择题 1mol水蒸气,18mL液态水(密度为1g/cm3),18g冰(密度为0.9g/cm3)中含的分子数是( )
A.水蒸气中最多
B.冰中最多
C.液态水中最多
D.一定相等
参考答案:D
本题解析:
本题难度:简单
4、选择题 设NA为阿伏加德罗常数的值,下列说法中正确的是(???? )。
A.2.4 g金属镁所含电子数目为0.2 NA
B.16 g CH4所含原子数目为NA
C.17 g NH3 所含质子数目为10 NA
D.18 g水所含原子数目为NA
参考答案:C
本题解析:A:镁原子含有12个电子,则2.4 g金属镁(即0.1 mol)含有电子为1.2 NA;B:CH4为五原子分子,16 g CH4也就是1 mol,应含有原子数目为5NA;C:NH3含有10个质子,所以17 g也就是1 mol,含有10 NA质子,正确;D:水为三原子分子,18 g水4也就是1 mol,应含有原子数目为3NA
本题难度:一般
5、选择题 室温下,抽去下图所示装置中的玻璃片,使两种气体充分反应。下列说法正确的是(设NA表示阿伏加德罗常数的值)

A.气体反应物的总体积为0.448L
B.装置中氢元素的总质量为0.04g
C.生成物中含有0.01NA个分子
D.生成物完全溶于永后所得溶液含有0.01 NA个NH4+
参考答案:B
本题解析:
试题分析:A、n(HCl)+n(NH3)=0.02mol,缺少标准状况下,不能确定反应前两种气体的体积,错误;B、n(H)=n(HCl)+3n(NH3)=0.04mol,由n×M可知m(H)=0.04g,正确;C、氯化氢与氨气刚好完全反应生成0.01mol氯化铵,NH4Cl是离子化合物,生成物中没有分子,错误;D、NH4Cl=NH4++Cl―,铵根离子水解,所得溶液中NH4+小于0.01mol,错误。
本题难度:一般