?
?
(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中。改进后的优点是________________________;
(4)验证CO的方法是____________________________;
参考答案:
(1) 本题解析:略 本题解析:略
本题难度:简单
2、实验题 过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,请填写下列空白:
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250mL??????????(填仪器名称)中,加水衡释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
?????MnO4-+?????H2O2+?????H+=????Mn2++?????H2O+□
(3)滴定时,将高锰酸钾标准溶液注入????????(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是??????????????。
(4)重 复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为????????????????????。 复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为????????????????????。
(5)下列操作能使测定结果偏高的是???????????
A.滴定前滴定管尖嘴中有气泡,滴定后气泡消失。
B.读取高锰酸钾标准溶液的刻度时,滴定前平视,滴定后俯视。
C.滴定前,在用蒸馏水洗涤滴定管后,未用高锰酸钾标准液润洗。
D.滴定过程中,锥形瓶中部分溶液溅出
参考答案:
 本题解析:略 本题解析:略
本题难度:一般
3、实验题 (14分)已知硝酸锏溶液颜色为蓝色.某学校化学课外小组同学们在做铜与浓硝酸、稀硝酸反应的实验中,发现铜和浓硝酸反应后溶液为绿色旦有红棕色气体产生,而铜和稀硝酸反应后溶液为蓝色,产生无色气体.为弄清反应后溶液颜色出现差异的原因,他们进行了实验探究.
[实验]在两支试管中各放入一小块等质量的铜片,分别加人等体积的浓HN03(14 mol ?
L-1)和稀HN03(4mol . L-1 ), 立即用蘸有NaOH的棉花封住试管口。充分反应后铜均无剩余。
(1) Cu与浓HNO3反应的离子方程式________________________________
(2) 用蘸有NaOH的棉花封住试管口的原因________________
已知NO2与NaOH溶液反应中,其中NO2的还原产物是亚硝酸盐(NO2-)
写出反应的化学反应式________________________,
[提出假设]假设一、因为铜离子浓度大造成的。
假设二、溶液呈绿色是因为铜与浓硝酸反应时产生的二氧化氮溶于过量浓硝酸,加上和蓝色的硝酸铜溶液混在一起,使溶液呈绿色。
[设计实验方案,验证假设]
(3) 上述实验________(“能”或“不能”)证明假设一不成立,原因________________
(4) 甲同学设计实验验证假设二,请帮他完成下表中内容(提示:NO3-在不同条件下的还咬产物较复杂,有时难以观察到气体产生)

[分析推理】
(5)铜和稀硝酸反应后溶液为蓝色的原理________________
参考答案:(14分)
 本题解析:略 本题解析:略
本题难度:一般
4、填空题 (10分)碳酸钙常用作牙膏 的摩擦剂。某同学设计了一种制备碳酸钙的方案,其流程图如下。(所用石灰石含有杂质SiO2) 的摩擦剂。某同学设计了一种制备碳酸钙的方案,其流程图如下。(所用石灰石含有杂质SiO2)

回答下列问题:
(1)充分煅烧110吨石灰石得到固体66吨,则石灰石中碳酸钙的质量分数为??????%。
(2)假设第①步反应完全进行,则第②步反应过滤后得到的不溶液性滤渣的成分为
?????????????????。
(3)第③步反应一般不采用通入CO2的主要原因是???????????????????????? ???,相应的离子方程式为?????????????????????????????????????。 ???,相应的离子方程式为?????????????????????????????????????。
(4)CaCO3是一种难溶液物质,25℃时其KSP=2.8×10-9。现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2.0×10-4mol/L,则生成沉淀所需CaCl2溶液的物质的量浓度最小是????????????????。
(5)某生用石灰石为原料,设计了另一种制备碳酸钙的实验方案,其流程图如下

与前一方案相比较,该方案的优点是???????????????。
参考答案:(10分).(1)90.9 (2分)???(2)CaSiO3
本题解析:略
本题难度:一般
5、实验题 工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移人硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________。
(2)另称取铁钉6.0g放入15.0ml.浓硫酸中加热,充分应后得到溶液X并收集到气体Y。 ①甲同学认为X中除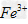 外还可能含有 外还可能含有 ?。若要确认其中的 ?。若要确认其中的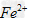 ?,应选用_____________。 ?,应选用_____________。
a.KSCN溶液和氯水?b.铁粉和KSCN溶液??c.浓氨水??d.酸性 溶液 溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:
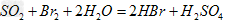 ?? ??
然后加入足量 溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中 溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中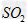 的体积分数为____________。 的体积分数为____________。
分析上述实验中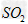 体积分数的结果,丙同学认为气体Y中还可能含量有 体积分数的结果,丙同学认为气体Y中还可能含量有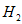 和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。?? 和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。??

(3)装置B中试剂的作用是_____________。
(4)认为?气体Y中还含有Q的理由是____________(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于___________?(选填序号)。 ?
?a.?A之前??????b.A-B间???????c.B-C间???????d.C-D间
(6)如果气体Y中含有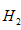 ?,预计实验现象应是______________。 ?,预计实验现象应是______________。
(7)若要测定限定体积气体Y中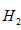 ?的含量(标准状况下约有 ?的含量(标准状况下约有 28ml??),除可用测量 28ml??),除可用测量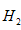 体积的方法外,可否选用质量称量的方法?做出判断并说明理由____________________. 体积的方法外,可否选用质量称量的方法?做出判断并说明理由____________________.
参考答案:(1)铁钉表面被钝化
(2)①d???????②66.
本题解析:
本题难度:困难
|