微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 (1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片上发生的电极反应:______;
银片上发生的电极反应:______.
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算:
产生氢气的体积(标准状况)______.
参考答案:(1)锌片、银片、稀硫酸构成原电池,锌作负极,负极上锌失电子
本题解析:
本题难度:一般
2、选择题 一种新型酸性乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍,电池反应式为C2H5OH + 3O2 =" 2" CO2 + 3H2O,电池构造如下图。下列关于该电池的说法不正确的是

A.放电过程中,电源内部的H+从正极区向负极区迁移
B.通入乙醇的电极是负极
C.该电池的正极反应为:4H+ + O2 + 4e-= 2H2O
D.用该电池做为电源,用惰性电极电解饱和NaCl的水溶液时,每消耗0.2 mol C2H5OH,阳极产生标准状况下气体的体积为26.88 L
参考答案:A
本题解析:
试题分析:放电时负极流出的电子通过外电路流入正极,电子带负电,则内电路中的阴离子从正极移向负极、阳离子从负极移向正极,故A错误;乙醇发生氧化反应,失去电子,所含碳元素的化合价升高,故B正确;酸性条件下氧气发生还原反应,得到电子,根据电子、电荷和原子守恒原理,故C正确;C2H5OH+3O2 =2CO2 +3H2O~12e-,则n(e-)转移=12×0.2 mol,阳极反应式为2Cl-―2e-=Cl2↑,根据电子守恒原理,则n(Cl2)= n(e-)转移/2=12×0.2 mol/2=1.2mol,V
本题难度:一般
3、选择题 某CH4燃料电池,工作环境是熔融的金属氧化物(MO),它能传导O2-,有关CH4燃料电池的说法中正确的是
A.电池内部电子从正极流向负极
B.负极电极反应式为:CH4-8e- + 10OH-=CO32-+ 7H2O
C.正极电极反应式为:O2 + 4e-=2O2-
D.每消耗22.4 L CH4,外线路中将通过8 mol电子
参考答案:C
本题解析:
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应,所以A不正确;B不正确,由于是熔融的盐作为电解质,则负极电极反应式是CH4-8e- +4O2-=CO2+ 2H2O;氧气在正极得到电子,生成氧离子,C正确;选项D中不能确定甲烷的状态,则22.4L甲烷不一定是1mol,D不正确,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,旨在培养学生分析、归纳和总结问题的能力,有利于调动
本题难度:一般
4、填空题 雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为____________。
(2)上述反应中的氧化剂是________?,反应产生的气体可用_________吸收。
(3)As2S3和HNO3有如下反应:As2S3+10H++10NO3-=2H3AsO4+?3S+10NO2↑+?2H2O 若生成2mol?H3AsO4,则反应中转移电子的物质的量为____________。若将该反应设计成一原电池,则NO2应该在_____________(填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L?O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量________(选填编号)。
a.小于0.5?mol????b.等于0.5?mol????c.大于0.5mol????d.无法确定
参考答案:(1)1:1
(2)As2S3;氢氧化钠(或硫酸铜溶液
本题解析:
本题难度:一般
5、填空题 (1)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备
甲醇。
Ⅰ:CH4 (g)+H2O(g)=CO(g)+3H2(g) ΔH="+206.0" kJ・mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g) ΔH=―129.0 kJ・mol-1
CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为
???????????????????????????????????????????????????????????????????。
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成C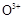 ,然后以C
,然后以C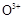 作氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置完成上述过程:
作氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置完成上述过程:
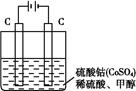
①写出阳极电极反应式: ?????????????????。
②写出除去甲醇的离子方程式: ??????????????????。
(3)写出以NaHCO3溶液为介质的Al―空气原电池的负极电极反应式: ????????????。
参考答案:(1)CH4(g)+H2O(g)=CH3OH(g)+H2(g
本题解析:(1)Ⅰ+Ⅱ得:CH4(g)+H2O(g)=CH3OH(g)+H2(g) ΔH="+77.0" kJ・mol-1。
(2)根据反应原理,通电后,将Co2+氧化成C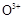 ,然后以C
,然后以C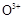
本题难度:一般