微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列电子式中错误的是( )
A.Na+
B.
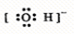
C.
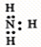
D.
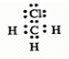
参考答案:C
本题解析:
本题难度:一般
2、选择题 X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增.已知X的最外层电子数是次外层电子数的3倍,X、M同主族,Y在同周期主族元素中原子半径最大.Z和N可以形成ZN2型化合物.下列有关说法正确的是( )
A.X与Y只能形成一种化合物
B.最高价氧化物对应水化物的碱性:Y>Z
C.气态氢化物的热稳定性:M>N
D.单质的氧化性:X<M
参考答案:X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数
本题解析:
本题难度:简单
3、选择题 下列说法正确的是( )
A.分子晶体中一定存在分子间作用力,不一定存在共价键
B.分子中含两个氢原子的酸一定是二元酸
C.含有金属离子的晶体一定是离子晶体
D.元素的非金属性越强,其单质的活泼性一定越强
参考答案:A、惰性气体组成的晶体中不含化学键,只含有分子间作用力,故A
本题解析:
本题难度:简单
4、填空题 (8分,每空2分)自从1962年首次合成了第一个稀有气体的化合物XePtF6以来,人们又相继发现了氙气的一系列化合物如XeF2、XeF4等。巴特列为开拓稀有气体化学作出了历史性贡献。
(1)请根据XeF4的结构示意图判断这个分子是极性分子还是非极性分子?_________??????????????。
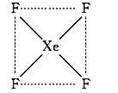
(2)XeF2晶体是一种无色晶体,下图为它的晶胞结构图。XeF2晶体属于哪种类型的晶体?_________;其堆积方式属于__________(填“钾型”“镁型”或“铜型”)。
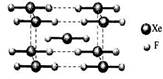
(3)一个XeF2晶胞中实际拥有XeF2__________个。
参考答案:(1)非极性分子 (2)分子晶体 钾型 (3)2
本题解析:(1)根据XeF4的结构示意图可判断,分子是平面正方形结构,所以是非极性分子。
(2)由于是由分子构成的,所以是分子晶体。根据晶胞结构可知,其堆积方式属于钾型。
(3)根据晶胞结构可知,一个XeF2晶胞中实际拥有XeF2是8×1/8+1=2。
本题难度:一般
5、选择题 已知结构为正四面体型的离子A和直线型离子B反应,生成三角锥形分子C和V形分子D(A、B、C、D均为10电子微粒,组成它们的元素原子序数均小于10),下列说法正确的是( )
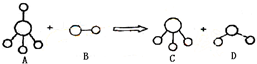
A.分子C与D不能发生化学反应
B.微粒A的空间结构与CH4相似,它们均为正四面体,所以A是非极性分子
C.固态D的熔沸点明显高于固态H2S的原因在于D分子中的共价键强于S-H键
D.在25℃时,A的盐酸盐溶液的pH小于7
参考答案:结构为正四面体型的离子A和直线型离子B反应,生成三角锥形分子
本题解析:
本题难度:简单