微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 (10分)下图为实验室某浓盐酸试剂瓶上的标签,

试根据有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为 mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.3 mol/L稀盐酸。
①该学生需要量取 mL上述浓盐酸进行配制。
②配制过程中,需要使用的仪器是(填写代号)________。
A.烧杯 B.量筒 C.1000 mL容量瓶 D.托盘天平
E.药匙 F.500 mL容量瓶 G.胶头滴管 H.玻璃棒
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) ;
A.用蒸馏水洗涤烧杯2―3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量蒸馏水的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻度线1―2cm处
参考答案:21.(10分)(1)12mol・L-1;(2)BD ;(3
本题解析:
试题分析:(1)浓盐酸中HCl的物质的量浓度为:c= =
=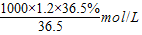 =12mol/L;
=12mol/L;
(2)取用任意体积的该盐酸溶液时,不同体积的溶液浓度相同,密度相同,答案为:B、D;
(3)①溶液稀释前后溶质的物质的量不变,设需浓盐酸的体积为V,则有12mol/L×V=0.5L×0.3mol/L,则V=0.0125L,及12.5ml,答案为:12.5;
②一般用量筒量取,在烧杯中稀释(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速稀释.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管.答案为:ABFGH;
③操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,所以配制时,其正确的操作顺序是BCAFED,答案为:BCAFED。
考点:考查一定物质的量浓度溶液的配制。
本题难度:一般
2、实验题 I.现有下图所示装置,为实现下列实验目的,其中应以a端作为入口的是 。

A.瓶内盛碱石灰,用以干燥气体
B.瓶内盛饱和食盐水,用以除去Cl2中混有的少量HCl
C.瓶内盛水,用以测量某难溶于水的气体体积
D.瓶内贮存气体,加水时气体可被排出
E.收集密度比空气大的气体
F.收集密度比空气小的气体
II.欲用98%的浓硫酸(密度为1.84g・cm-3)配制浓度为1mol・L-1的稀硫酸480mL。
(1)从下列用品中 选出实验所需要的仪器
A.1000mL烧杯 B.100mL烧杯 C.10mL量筒 D.50mL量筒
E.500mL容量瓶 F.1000mL容量瓶 G.广口瓶 H.托盘天平
(2)除选用上述仪器外,还缺少的必要仪器或用品是
(3)需取用浓硫酸的体积为 mL (结果保留一位小数)
(4)下列情况中,会使所配溶液的浓度偏低的是
A.将量筒中的浓硫酸转入烧杯后,用水洗涤量筒,将洗液也转入在烧杯中
B.稀释浓硫酸后立即转入容量瓶
C.定容时加水不慎超过刻度线
D.定容时仰视刻度线
参考答案:(共12分)I.BDE (3分) (错选、少选一个
本题解析:
试题分析:I.装置是长进短出,充入的气体密度要大于排出气体的密度,故BDE正确。
II. (1)配置溶液选用的仪器有烧杯、量筒、容量瓶、玻璃棒、胶头滴管,选择具体大小的仪器(玻璃棒除外)应根据所配溶液的量,故BDE是正确的。
(2)根据(1)可知缺少的是玻璃棒和胶头滴管。
(3)利用公式V=m/?="(nM)/" ?=[cV(溶液)M[/ ?,需取用浓硫酸的体积为27.2 mL。
(4)A项:不用洗涤量筒,否则偏大,故错;B项:应冷却后转入容量瓶,否则偏大,故错。故选CD。
考点:溶液的配置及误差分析
点评:本题重点考查的是溶液的配置及误差分析的相关知识,题目难度大,注意实验中的小细节是解题的关键。
本题难度:一般
3、选择题 铁、镁、铝三种金属分别和等体积等浓度的盐酸反应,同温同压下,产生相同体积的氢气,则
A.金属失去的电子数相等
B.参加反应的金属质量相等
C.参加反应的金属物质的量相等
D.铁、镁、铝的质量比为56:24:27
参考答案:A
本题解析:三种金属与盐酸反应的方程式分别是Fe+2H+=Fe2++H2↑、Mg+2H+=Mg2++H2↑、2Al+6H+=2Al3++3H2↑,所以选项A正确,其余都是错误的,参加反应铁、镁、铝的质量比为56:24:18,所以正确的答案选A。
本题难度:一般
4、选择题 把500mL有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为
A.0.1(b-2a)mol/L
B.10(2a-b)mol/L
C.10(b-a)mol/L
D.10(b-2a)mol/L
参考答案:D
本题解析:
试题分析:取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀,表明每一份中含钡离子为a mol;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀,表明每一份中含氯离子b mol,由此可知,每一份溶液中含有的钾离子为(b-2 a)mol,那么原溶液中所含的钾离子为5(b-2 a)mol,其浓度为10(b-2a)mol/L。
本题难度:简单
5、选择题 相同温度下,在两个等体积的密闭容器中,分别充入氦气、氮气两种气体,当他们的密度都相同时,这两种气体的物质的量之比是
A.1 : 7
B.2 : 7
C.7 : 1
D.7 : 2
参考答案:C
本题解析:略
本题难度:一般