微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 已知由短周期常见元素形成的纯净物A、B、C、D、E、F、X转化关系如下图所示,B、X为单质,D常温下为无色液体,A、B含同一种元素。(某些产物可能略去)
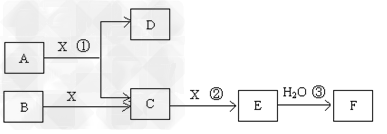
请回答下列问题:
(1)若E是有色气体,F是一元强酸,反应①是工业制备F的第一步反应。
①写出A与X反应的化学方程式:??????????????????????????。
②有人认为“浓H2SO4可以干燥气体E”。某同学为了验证该观点是否正确,用下图装置进行实验。实验过程中,浓H2SO4中未发现有气体逸出,且浓H2SO4由无色变为红棕色,由此你得出的结论是???????????????????????????? 。

③已知常温下1 mol气体E发生反应③放出46kJ热量,写出气体E与H2O反应的热化学方式______________ 。
④在常温下,向V1L pH=a的A溶液中加入V2L pH=b的盐酸,且a+b=14,若反应后溶液的pH<7,则V1和V2的关系为V1________V2(填>、<、无法确定),所得溶液中各种离子的浓度由大到小的顺序可能是_________ 。(写出一种情况即可)
(2)若E为无色无味气体,F是二元弱酸。
①E的电子式为 ___________;
②将少量气体E通入氢氧化钡溶液中得不溶物F,F的KSP=8.1×10-9。现将该沉淀放入0.1mol/L的BaCl2溶液中,其KSP_____________,(填:增大、减小或不变),此时,组成不溶物F的阴离子在溶液中的浓度为 _____mol/L。
参考答案:(1)①氨气的催化氧化反应方程式“略”
???????
本题解析:
本题难度:一般
2、填空题 有关元素X、Y、Z、W的信息如下:

请回答下列问题:
(1) Y的单质在空气 中充分燃烧所得氧化物的电子式________________
中充分燃烧所得氧化物的电子式________________
(2) X、Y、W的简单离子的半径由大到小的是_______________ (写离子符号)
(3) 向淀粉碘化钾溶液中滴加几滴 的浓溶液,现象为______________ ,
的浓溶液,现象为______________ ,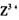 基态离子的电子排布式为????
基态离子的电子排布式为????
(4) 以 溶液为原料制取无水
溶液为原料制取无水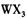 ,主要操作包括加热浓缩、冷却结晶、过滤,先制得
,主要操作包括加热浓缩、冷却结晶、过滤,先制得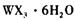 晶体,然后在条件下加热
晶体,然后在条件下加热 晶体,能进一步制取无水
晶体,能进一步制取无水 .其原因是(结合离子方程式简要说明)???? _____________________________________________
.其原因是(结合离子方程式简要说明)???? _____________________________________________
参考答案:(12分)
 本题解析:略
本题解析:略
本题难度:一般
3、简答题 已知①~④均为工业生产及应用的常见反应.其中常温下B、D、J、P气体,E为分子中原子个数比为1:l的液体.A的相对分子质量为120.(个别反应的产物已略去)
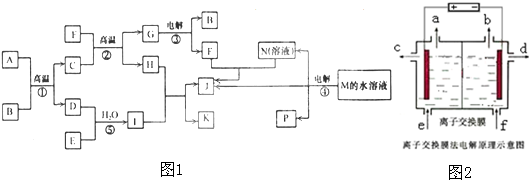
试回答下列问题:
(1)反应F与N溶液反应的离子方程式为______;
(2)反应⑤中当有1mol电子转移时,氧化剂消耗______g;
(3)反应④的离子方程式为______;如图2是该反应原理的示意图,该装置中使用的是______(填“阴”或“阳”)离子交换膜,图中从d处收集到的是______.
(4)工业上由D制取I的过程可表示为:
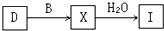
由D与B反应生成X的反应所用的设备是______;
①高炉???????②沸腾炉????????③接触室???????④分馏塔?????⑤吸收塔
已知400℃101Kpa时,2D(g)+B(g?2X(g);△H=-196.6KJ/mol,当2mol?D与1mol?B在该条件下反应达平衡时反应放热186.8KJ.在实际生产中综合考虑各种因素,为提高D的转化率,工业选择了以下哪些条件______.
①适当升高温度????②增大压强?????③使用合适的催化剂???? ④及时移走生成物????????
⑤适当增大B的浓度??????⑥将反应物与生成物在热交换器中进行热交换.
参考答案:(1)反应F(Al)与N(NaOH)溶液反应的离子方程式为:
本题解析:
本题难度:一般
4、选择题 一定条件下,中学化学常见物质,甲、乙、丙、X之间存在“甲
X
乙X
丙”的转化关系,丙不可能是( )
A.SO3
B.Si
C.CO
D.FeCl2
参考答案:B
本题解析:
本题难度:一般
5、选择题 元素A的单质及A与B形成的化合物能按如下图所示的关系发生转化.则下列说法正确的是( )
A.图中物质间的转化可能有非氧化还原反应
B.当n=1时,A可能是N2
C.A一定是金属元素
D.当n=2时,A可能是Fe
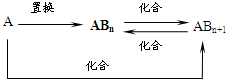
参考答案:D
本题解析:
本题难度:一般