微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知室温时,0.1mo1/LCH3COOH在水中有0.1%发生电离,下列叙述正确的是:
A.该溶液的pH=5
B.由CH3COOH电离出的c(H+)约为水电离出的c(H+)的106倍
C.CH3COOH的电离平衡常数约为1×10-6
D.升高温度,溶液的pH增大
参考答案:B
本题解析:
试题分析:0.1mo1/LCH3COOH在水中有0.1%发生电离,即c(H+)= c(CH3COO-)=0.1%×0.1mo1/L=10-4 mo1/L。pH=4,A不正确;因Kw=c(H+)・c(OH-)水=10-14,故c(OH-)水=c(H+)水=10-10 mo1/L,B正确;Ka= c(H+)・c(CH3COO-)/ c(CH3COOH)= 10-4×10-4/(0.1-10-4)= 1×10- 本题难度:一般
本题难度:一般
2、选择题 下列溶质的溶液中,pH>7的是:
A.KNO3
B.CH3COONa
C.NaHSO4
D.AlCl3
参考答案:B
本题解析:略
本题难度:简单
3、填空题 化学平衡移动原理同样适用于其他平衡。已知在氨水中存在下列平衡:
NH3+H2O NH3・H2O
NH3・H2O 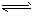 NH4++OH-
NH4++OH-
(1)向氨水中加入MgCl2固体时,平衡向____移动,OH-离子的浓度____,NH4+离子的浓度____。
(2)向氨水中加入浓盐酸,平衡向____移动,此时溶液中浓度减小的微粒有____、 ____、_____。
(3)向浓氨水中加入少量的NaOH固体,平衡向_______移动,此时发生的现象是________。
参考答案:(1)正反应方向 ;减小 ;增大
(2)正反应方向
本题解析:
本题难度:一般
4、选择题 已知25℃时有关弱酸的电离平衡常数:
弱酸
| CH3COOH
| HCN
| H2CO3
|
电离平衡常数
| 1.8×l0-5
| 4.9×l0-10
| K1=4.3×l0-7??K2=5.6×l0-11
?
25℃下,下列有关说法正确的是
A.浓度为0.1mol/L的HCN溶液中c(OH-)=10-13mol/L
B.物质的量浓度相同的稀酸溶液中KW:CH3COOH>H2CO3>HCN
C.物质的量浓度相同的三种钠盐溶液的pH:NaHCO3>NaCN>CH3COONa
D.浓度均为amol?L-1HCN溶液与NaOH溶液等体积混合充分反应后的溶液中(忽略体积的变化)c(H+)<c(OH-)<c(CN-)<0.5amol/L
参考答案:D
本题解析:
试题分析:A、根据电离平衡常数可知,HCN的酸性弱于醋酸的,因此HCN是弱酸,则浓度为0.1mol/L的HCN溶液中c(OH-)>10-13mol/L,A不正确;B、水的离子积常数只与温度有关系,常温下物质的量浓度相同的稀酸溶液中KW:CH3COOH=H2CO3=HCN,B不正确;C、根据电离平衡常数可知,酸性强弱顺序是CH3COOH>H2CO3>HCN。由于酸越弱,相应的钠盐越容易水解,溶液的碱性越强,所以物质的量浓度相同的三种钠盐溶液的pH:NaCN>NaHCO3>CH3COONa,C不正确;
本题难度:一般
5、实验题 (8分)为了证明一水合氨是弱电解质,甲、乙、丙、丁四位学生利用下面的试剂进行实验:0.10 mol・L-1氨水、NH4Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.10 mol・L-1氨水pH为10, 据此他认定一水合氨是弱电解质,你认为这一结论_________(填正确或不正确或无法确定),并说明理由______________________________________________
(2)乙取出10 mL 0.10 mol・L-1氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000 mL,再用pH试纸测出其pH为b,他认为只要a、b值应满足如下关系_______________(用等式或不等式表示)就可以确认一水合氨是弱电解质。
(3)丙取出10 mL 0.10 mol・L-1氨水,滴入2滴酚酞试液,显粉红色,再加入CH3COONH4晶体少量,颜色变浅;你认为这一方法能否证明一水合氨是弱电解质______(填能或否)。
(4)丁同学的方案最可能是(答出实验原理、现象与结论)______________________
参考答案:(每小题2分)(1)正确;常温下,对0.1 mol・L―1
本题解析:0.1mol/L的一元强碱溶液的pH=13,而弱酸溶液的pH因其不能完全电离而小于13,故方法一的判断是正确的。0.1mol/L的强碱溶液稀释100倍后,其中pH会减小2个单位,弱碱则因稀释会促进原来没有电离的酸分子又电离出一部分H+而导致pH减小值小于2个pH单位。因少量晶体的加入对溶液体积的影响可以忽略不计,故溶液颜色变浅只能是由于平衡移动导致溶液中OH-减小导致的,故以此现象可以判断该碱是弱电解质。由于还有强酸盐NH4Cl,故最可能是测量其溶液的pH。
本题难度:简单
|