微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 工业上采用湿法炼锌过程中,以ZnSO4为主要成分的浸出液中,含有Fe3+、Fe2+、Cu2+、Cl-等杂质,这些杂质对锌的电解工序有妨碍,必须事先除去。现有下列试剂可供选择:①酸性KMnO4溶液 ②NaOH溶液 ③ZnO ④H2O2溶液 ⑤Zn ⑥Fe ⑦AgNO3 ⑧Ag2SO4下列说法不正确的是 [???? ]
A.用酸性KMnO4溶液将Fe2+氧化成Fe2+,再转化为Fe(OH)3沉淀除去
B.用ZnO调节浸出液的酸碱性,可使某些离子形成氢氧化物沉淀
C.在实际生产过程中,加入Ag2SO4可除去Cl-,是利用了沉淀转化的原理
D.也可以用ZnCO3代替ZnO调节溶液的酸碱性
2、选择题 冶炼金属一般有下列四种方法:
① 焦炭法 ② 水煤气(或CO、或H2)法 ③ 活泼金属置换法 ④ 电解法。
四种方法在工业上均有应用。
古代有:(1)火烧孔雀石炼铜;(2)湿法炼铜。
现代有:(3)铝热法炼铬;(4)从光卤石中炼镁。
其中对它们的冶炼方法的分析不正确的是[???? ]
A.(1)①
B.(2)②
C.(3)③
D.(4)④
3、填空题 已知反应?①、②?是化工生产中的两个重要反应:
①?甲溶液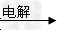 ?A?+?B?+?C
?A?+?B?+?C
②?乙经过粉碎后在沸腾炉中燃烧,得到D和E 其中,A、D在常温常压下为刺激性气味气体,C为无色无味气体。
请回答:
(1)A的电子式是_____________。?????
(2)将A通入B的溶液中,反应的离子方程式是__________。?
(3)1?g?C在A中燃烧时放出92.3?kJ的热量,该反应的热化学方程式是___________。
(4)工业上可利用E为原料冶炼其中所含的金属,方法是_____________。
(5)化工生产②中第二步、第三步用到的设备名称分别为_________、___________。第二步采用的反应条件为______________。
(6)将A和D按物质的量1:1通入下列装置中:? 该过程中的化学方程式是_____________?。上述实验装置设计不完整,请将所缺部分在装置图的下边方框中画出。
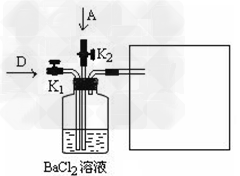
(7)一定条件下,将12?g乙放入过量的的浓硝酸中,反应过程中转移1.5?mol电子,该反应的离子方程式是______________。???
4、填空题
【三选一―选修化学与技术】???
(1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。 ??
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2??的化学方程式:___;???
②写出“联合制碱法”有关反应的化学方程式:____; ??
③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?____??
(2)钢铁工业对促进经济和社会发展起了重要作用。 ??
①炼钢时,加入硅、锰和铝的目的是___; ??
②不锈钢含有的铬元素是在炼钢过程的氧吹___(填“前”或“后”)加入; ??
③炼铁和炼钢生产中,尾气均含有的主要污染物是___;从环保和经济角度考虑,上述尾气经处理可用作___。
5、选择题 分别用氢气和金属做还原剂冶炼金属,下列关于所得到金属的纯度的说法,正确的是[???? ]
A.用氢气的纯度高
B.用金属的纯度高
C.二者相同
D.无法比较