微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答
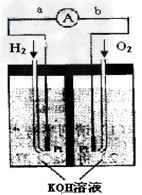
(1)氢氧燃料电池的能量转化主要形式是__________,在导线中电子流动方向为___________(用a、b?表示)。
(2)负极反应式为__________。
(3)电极表面镀铂粉的原因为_______________。
参考答案:(1)化学能转变电能??;a流向b??
(2)H2-
本题解析:
本题难度:一般
2、填空题 有如下两个反应:
A? 2HCl+Ba(OH)2===BaCl2+2H2O
B? 2Fe3++Cu==2Fe2++Cu2+
(1) 根据两反应的本质,判断能否设计成原电池:A?????B??????(填“能”或“不能” )不能设计成原电池的原因是????????????????????????????????????????????????????
(2) 根据能设计成原电池的反应选择适合的材料和试剂设计一个原电池
①负极材料是_______,正极材料是________,电解质溶液是??????? ___;
②写出负极的电极反应式???????????????????????????????????????? _;
③原电池工作时溶液中的Cl-从__________极向________极移动(填正或负)
④若导线上转移电子0.2mol,则负极质量变化是??? ___ 减少??? ___???;
 ?将此反应设计成原电池,若电解质溶液为H2SO4,
?将此反应设计成原电池,若电解质溶液为H2SO4,
请写出正负极的电极反应;负极:_______________;正极:______________。
参考答案:(15分)(1)A不能,B能,A不是氧化还原反应(每空1分)
本题解析:
试题分析:(1)只有氧化还原反应才能设计生成原电池,A是中和反应,不能设计成原电池。B是氧化还原反应,可以设计成原电池。
(2)①根据B的方程式可知,铜失去电子,被氧化,则负极一定是铜,而正极材料可以是石墨等。铁离子得到电子,发生还原反应,则电解质溶液应该是氯化铁溶液。
②负极的电极反应式是Cu-2e===Cu2+。
③原电池工作时溶液中的Cl-从正极向负极移动。
④若导线上转移电子0.2mol,则负极质量减少0.1mol×64g/mol=6.4g。
(3)根据反应式
本题难度:一般
3、选择题 根据下图,下列判断中正确的是
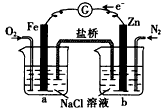 [???? ]
[???? ]
A.烧杯a中的溶液pH 升高
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-=H2
D.烧杯b中发生的反应为2Cl--2e-=Cl2
参考答案:AB
本题解析:
本题难度:一般
4、选择题 在用Zn、Cu片和CuSO4溶液组成的原电池装置中,经过一段时间工作后,下列说法中正确的是
A.锌片是正极,铜片质量不变
B.电流方向是从锌片流向铜片
C.锌片是负极,铜片质量不变
D.锌片是负极,铜片质量增加
参考答案:D
本题解析:用Zn、Cu片和CuSO4溶液组成的原电池,锌比铜活泼,锌做负极,失电子,锌片质量减小,铜做正极,溶液中的铜离子得电子在正极山析出,质量增加,故选D。
本题难度:简单
5、选择题 根据下图,下列判断中正确的是(? )
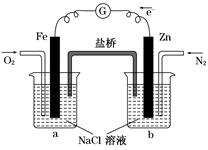
A.烧杯a中的溶液pH升高
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-=H2
D.烧杯b中发生的反应为2Cl--2e-=Cl2
参考答案:AB
本题解析:由图知,烧杯b中的Zn棒失去电子,发生氧化反应,电子转移到Fe棒上,烧杯a中通入的氧气在Fe棒表面得电子生成氢氧根离子,使a中溶液的pH升高。所以正确的为A、B。
本题难度:一般