微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分)今有Fe和Zn的混合物12.1g,与足量的稀盐酸反应,共放出H2 4.48L(标准状况)。求:
(1)原混合物中Fe的质量分数。
(2)消耗HCl的物质的量。
参考答案:(1) m(Fe)="5.6g???" 46.3% (3分)
本题解析:略
本题难度:简单
2、推断题 C、E是中学化学中常见的单质,A是固体,C、E 是无色无味的气体,D是黑色晶体,它们之间的转化关系如下图所示。

(1)写出A、B、C的化学式:A___,B___,C___。
(2)写出A、B转化为D、E的化学方程式:___。
(3)写出D与浓盐酸反应的离子方程式:___。
参考答案:(1)Fe ;H2O ;O2
(2)3Fe+4H2O
本题解析:
本题难度:一般
3、选择题 铁片放入下列溶液中,反应时无气体放出,取出后铁片质量减轻,则该溶液是
A.稀硫酸
B.CuSO4
C.AgNO3
D.Fe2(SO4)3
参考答案:D
本题解析:
试题分析:铁和稀硫酸反应生成硫酸亚铁和氢气;和硫酸铜反应生成硫酸亚铁和铜,铁片的质量增加;铁和硝酸银溶液反应,生成硝酸亚铁和银,铁片的质量增加;铁和硫酸铁反应生成硫酸亚铁,铁片的质量减少,答案选D。
点评:该题是高考中的常见考点之一,主要是检验学生对铁单质化学性质的熟悉掌握程度,以及灵活运用知识的能力。
本题难度:一般
4、选择题 在稀硫酸中加入铜粉,铜粉不溶,再加入下列固体粉末:①FeCl2; ②Fe2O3; ③Na; ④Ca(NO3)2。铜粉可溶解的是(???)



 ?
?
A.①②
B.②④
C.②③
D.①④
参考答案:B
本题解析: 加入Fe2O3反应生成Fe3+能氧化铜,加入Ca(NO3)2后等于铜和硝酸反应而消耗。
加入Fe2O3反应生成Fe3+能氧化铜,加入Ca(NO3)2后等于铜和硝酸反应而消耗。
本题难度:一般
5、填空题 铁黄是一种重要的颜料,化学式为Fe2O3・xH2 O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含FeZ 0。及少量的CaO, Mg0等)和黄铁矿粉
(主要成分为FeS2)制备铁黄的流程如下:
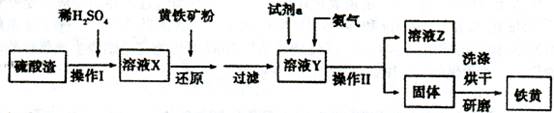
(1)操作I与操作II中都用到玻璃棒,玻璃棒在两种操作中的作用分别是_?????、??????
(2)试剂a最好选用_???(供选择使用的有:铝粉、空气、浓HNO3 );其作用是_???????????。
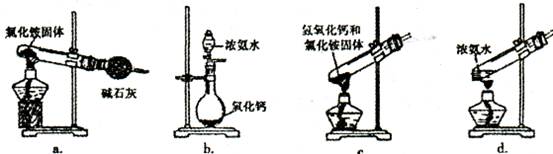
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是_???????_(填序号)。
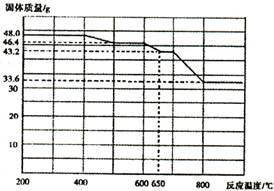
(4)查阅资料知,在不同温度下Fe2 O3被CO还原,产物可能为Fe3 O4?、FeO或Fe,固体质量与反应温度的关系如右图所示。根据图象推断670℃时Fe2 O3还原产物的化学式为M,并设计一个简单的实验,证明该还原产物的成分(依次填写每步操作中所加试剂的化学式、现象和结论)。仪器自选。可供选择的试剂:稀H2SO4、稀盐酸、H2 O2溶液、NaOH溶液、KSCN溶液。
加入试剂
| 现象
| 结论
|
?
| ?
| 则还原产物为?????
|
?
| ?
|
?
| ?
?
参考答案:
(1)搅拌加速溶液;引流。(2)空气;作氧化剂,将二
本题解析:
试题分析:(1)操作I是搅拌加速溶液溶解,操作II是过滤操作,主要用到玻璃棒引流。(2)试剂a最好选用空气,来源廉价,其作用是作氧化剂,将二价铁离子氧化为三价铁离子。(3)实验室制氨气的主要是操作简单,制作方便,由于氨气易溶于水,故要加热,可选择bd。(4)对于二价铁离子有无可用KSCN溶液不显红色判断,对于有无固体铁可用加入酸有无气泡做出判断。CO还原氧化铁的还原产物为可能Fe3O4,FeO和Fe,Fe2O3加热温度可达到500℃~600℃,质量由46.4g减少为45g,还原产物为Fe3O4;6
本题难度:困难
|