��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��Դ���ִ�������ԭ������ͨ����ѧ��������ʹ��������������������ʽת�����Ӷ���������Դ�������Դ�������ʣ�
��1��������ȼ��ʱ���ų�����������˵���÷�Ӧ��______�ȷ�Ӧ���������ڷ�Ӧ���������______�������������������ڡ�����С�ڡ����ڡ�����ͬ�����ӻ�ѧ��Ӧ�ı��ʽǶ������������ڶ��ѷ�Ӧ���еĻ�ѧ�����յ�������______�γɲ���Ļ�ѧ���ų�����������
��2������������Ϊ��21���ʹ������ȼ�ϵ�������Դ��5.2g����ȼ��ʱ�ų�286kJ��������ÿǧ������ȼ��ʱ�ų�������Ϊ46000kJ���Ծݴ˷���������Ϊ��Դ�������͵�����
______��
��3��ͨ��������ȼ�շ�Ӧ�������������̺��Ļ�ѧ��ת��Ϊ���ܣ��������������ԭ��Ӧ��Ƴ�ԭ���װ�ã��Ϳ����������̺��Ļ�ѧ��ת��Ϊ���ܣ���ͼ�����ܹ�ʵ�ָ�ת����װ�ã�����Ϊ����ȼ�ϵ�أ��õ�ص�������______����a�缫��b�缫������缫��ӦΪ______��
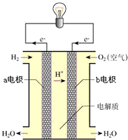
�ο��𰸣���1��ȼ�շ�Ӧ���Ƿ��ȷ�Ӧ������������ȼ�շ�Ӧ�Ƿ��ȷ�Ӧ����
���������
�����Ѷȣ�һ��
2��ѡ���� ��ӦC��ʯī��?C�����ʯ�������ȷ�Ӧ���ɴ˿�֪��������
A��ʯī�Ƚ��ʯ���ȶ�
B�����ʯ��������ʯī�ĵ�
C�����ʯ��ʯī�ȶ�
D�����ʯ��ʯī�����ת��
�ο��𰸣�A��ʯīת��Ϊ���ʯҪ����������˵��ʯī�������ͣ��ȶ�����A
���������
�����Ѷȣ���
3��ѡ���� ����˵���У�������ǣ�???��
A������Ŀǰ��ֱ�����õ����������ɻ�ѧ��Ӧ������
B��ú��ʯ�͡���Ȼ���ǵ�����������Ҫ�����ֻ�ʯȼ��
C���ҹ�Ŀǰ����Ҫ����Դ��ú̿
D�������˶������ĵ������뻯ѧ��Ӧ��
�ο��𰸣�D
�����������������ʱ�̶��ڽ��г�ǧ����Ļ�ѧ��Ӧ�����������ṩ�˶����������
�����Ѷȣ���
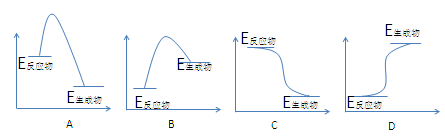
4������� ������ķ�ͼ���������ĸ���Ӧ��һһ��Ӧ��ϵ�������ҳ�������������ı����У�
��HCl + NaOH ��NaCl + H2O + Q??????��H2 + Cl2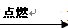 2HCl + Q
2HCl + Q
��CaCO3 �� CaO + CO2�� - Q?????????��Ba(OH)2��8H2O �� Ba(OH)2 + 8H2O �C Q
��
| ��
| ��
| ��
|
?
| ?
| ?
| ?
�ο��𰸣�
��
��
��
��
C
A
���������
�������������ͼ���֪��A��C�з�Ӧ������������������������������Ӧ�Ƿ��ȷ�Ӧ����A�з�Ӧ����Ҫ��������������Ϊԭ�ӣ�����A��Ӧ���Ǣڣ�C��Ӧ���Ǣ١�B/D�з�Ӧ���������������������������������ȷ�Ӧ������B�з�Ӧ����Ҫ��������������Ϊԭ�ӣ�����B��Ӧ�ۣ�D��Ӧ�ܡ�
�����������dz�ʶ��֪ʶ�Ŀ��飬���������ӱ��������ǿ��ּ�ڹ���ѧ���Ļ��������ѧ��������������Ĺؼ�����ȷ��Ӧ�ȵĺ����Լ���Ӧ�ȴ�С���ж����ݣ�Ȼ����ͼ��������ü��ɡ�
�����Ѷȣ�һ��
5������� (1)��֪���������Ȼ�ѧ����ʽ��
C3H8(g)+5O2(g) =3CO2(g)+4H2O(l)?��H=��2220.0 kJ��mol-1
H2O��l��=H2O��g��?��H="+44.0" kJ��mol-1
��0.5mol����ȼ������CO2����̬ˮʱ�ͷŵ�����Ϊ?????????????��
(2)��֪��TiO2(s)��2Cl2(g)=TiCl4(l)��O2(g)??��H����140 kJ��mol��1
2C(s)��O2(g)="2CO(g)" ��H����221 kJ��mol��1
д��TiO2�ͽ�̿��������Ӧ����TiCl4��CO������Ȼ�ѧ����ʽ��????????????��
(3)��ѧ���ѻ���˼��������о������N4���ӣ���ṹΪ�������壨��ͼ��ʾ��������������ơ���֪����1molN��N������193kJ����������1molN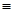 N������941kJ��������1molN4����ת��Ϊ2molN2ʱҪ�ų�??????????????kJ������ N������941kJ��������1molN4����ת��Ϊ2molN2ʱҪ�ų�??????????????kJ������

��4������������ɴ���ʹ�õ�������ȼ�ϵ�أ������ܷ�ӦΪ��2H2+O2��2H2O���������ҺΪϡH2SO4��Һ����طŵ�ʱ�ǽ�?????��ת��Ϊ?????�ܡ���缫��Ӧʽ�ֱ�Ϊ������????????????????������???????????????????��
�ο��𰸣���1�� 1022kJ?��2�� TiO2(s)��2Cl2(g)
���������
�����������1����֪��C3H8(g)+5O2(g)��3CO2(g)+4H2O(l)?��H=��2220.0 kJ��mol-1����H2O��l����H2O��g��?��H="+44.0" kJ��mol-1������ݸ�˹���ɿ�֪��+�ڡ�4���õ�C3H8(g)+5O2(g)��3CO2(g)+4H2O(g)?��H=��2044kJ��mol-1����0.5mol����ȼ������CO2����̬ˮʱ�ͷŵ�����Ϊ2044kJ��mol-1��0.5mol��1022kJ��
��2����֪����TiO2(s)��2Cl2(g)��TiCl4(l)
�����Ѷȣ�һ��
|