微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)在以铁、铜为两电极的原电池中,如图所示:
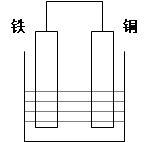
(1)若电解质溶液为稀硫酸,则铜电极上的电极反应式为: ;原电池总反应的离子方程式: ;
(2)若电解质溶液为浓硝酸, 则铁电极上的电极反应式为: ;当电路中通过了1mol的电子时,则在某极上生成了标准状况下的气体体积为: L。
参考答案:(1) 2H++2e-= H2↑;2
本题解析:(1)在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。铁比铜活泼,铁是负极,铜是正极,溶液中的氢离子得到电子。
(2)如果是浓硝酸,由于铁会发生钝化,所以作负极的是铜,失去电子而溶解。铁是正极,溶液中的NO3-得到电子,反应式为NO3-+2H++e-= NO2↑+ H2O。根据电极反应式可知,当电路中通过了1mol的电子时,生成NO2的体积在标准状况下为22.4L。
本题难度:一般
2、选择题 把金属A和金属C分别投入到等浓度的盐酸中,A比C反应剧烈;A与金属B组成原电池时,A为电池的正极。A、B、C三种金属的活动性顺序为
A.A>C>B B.A>B>C C.B>A>C D.B>C>A
参考答案:C
本题解析:
试题分析:金属越活泼,越容易和盐酸反应,反应就越剧烈,所以A的金属性强于C的;原电池中较活泼的金属是负极,失去电子,发生氧化反应,所以根据A与金属B组成原电池时,A为电池的正极可知,金属性是B大于A,则A、B、C三种金属的活动性顺序为B>A>C,答案选C。
考点:考查元素金属性强弱的判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,难易适中。在注重对基础知识巩固和训练的同时,侧重对学生能力的培养和训练。该题的关键是明确金属性强弱比较的规律,特别是利用原电池原理比较金属性强弱的规律,有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:简单
3、选择题 如下是某原电池的结构示意图,下列说法不正确的是(盐桥中装满用饱和KCl溶液和琼胶做成的冻胶)
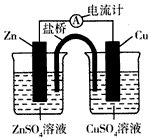 [???? ]
[???? ]
A.该原电池反应为Zn+Cu2+=Zn2+ +Cu
B.该电池工作时,Zn电极失去电子,发生氧化反应
C.该电池工作一段时间后,CuSO4溶液蓝色变浅
D.盐桥中的K+移向ZnSO4溶液,Cl-移向CuSO4溶液
参考答案:D
本题解析:
本题难度:一般
4、填空题 选择适宜的材料和试剂设计一个原电池,完成下列反应:
Zn+CuSO4=ZnSO4+Cu
(1)画出装置图:______
(2)电极材料和电解质溶液各是什么?______
(3)写出电极反应式:
正极:______;负极:______.
参考答案:(1)根据自发的氧化还原反应:金属锌失电子,为负极,正极可以
本题解析:
本题难度:一般
5、选择题 X、Y、Z、M代表四种金属元素。金属X和Z用导线连接放入稀硫酸中时,Z极上有H2放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为 ( )
A.X>Z>Y>M
B.X>Y>Z>M
C.M>Z>X>Y
D.X>Z>M>Y
参考答案:A
本题解析:略
本题难度:一般