微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 已知pH为4-5的条件下,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(n)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,过程如下
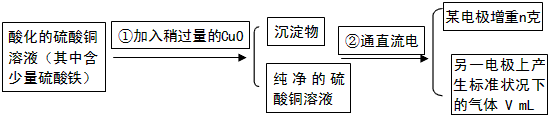
回答下列问题:
(1)加入CuO的作用是_______________________。
(2)步骤②中所用的部分仪器如下图所示,则A、B分别连直流电源的__________和__________极(填“正”或“负”)。
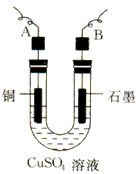
(3)电解开始后,在U形管中可以观察到的现象有:________________________
电解的离子方程式(总反应)为________________________。
(4)下列实验操作中必要的是____________(填写字母)。
(A)称量电解前的电极的质量;
(B)电解后,电极在烘干称量前,必须用蒸馏水冲洗;
(C)刮下电解后电极上析出的铜,并清洗,称量;
(D)电解后烘干称重的操作中必须按“烘干→称量→再烘干→ 再称量”进行;
(E)在有空气存在的情况下,烘干电极必须用低温烘干的方法。
(5)铜的相对原子质量为_______________________(用带有n、V的计算式表示)。
参考答案:(1)通过消耗H+而调整溶液的pH使之升高,其目的是使Fe3
本题解析:
本题难度:一般
2、选择题 用阳极甲、阴极乙、电解质溶液丙,在电解过程中补充加入丁物质,可以使电解液的组成保持恒定(物质和浓度与电解前完全相同),下列答案正确的是(??)
?
| 甲
| 乙
| 丙
| 丁
|
A
| Pt
| Pt
| CuCl2
| HCl气体
|
B
| C
| Cu
| CuSO4
| CuO固体
|
C
| Pt
| C
| H2SO4
| H2SO4(纯)
|
D
| Fe
| Fe
| NaCl
| NaOH固体
参考答案:B
本题解析:考查电极产物的判断。选项A中电极产物是铜和氯气,因此需要加入氯化铜;选项B中电极产物是铜、氧气和硫酸,所以需要加入氧化铜;选项C中电极产物是氢气和氧气,因此需要加入水;选项D中铁是阳极失去电子,阴极是溶液中的氢气得到电子,所以生成物是氢气和氢氧化亚铁,所以选项D不正确,答案选B。
本题难度:一般
3、选择题 下列关于电解法精炼粗铜的叙述中正确的是
A.精铜板作阴极,粗铜作阳极,CuSO4溶液作电解液
B.电解时,阴极发生氧化反应,则阴极发生的反应为:Cu2+ +2e― ==Cu
C.粗铜中所含Ni.Fe.Zn等金属杂质,电解后以单质形式沉积槽底,形成阳极泥
D.两电极质量变化值相等
参考答案:A
本题解析:精炼铜时:
阳极失电子,发生氧化反应:Cu ―2e― ==Cu2+(Fe ―2e― ==Fe2+等)
阴极得电子,发生还原反应:Cu2+ +2e― ==Cu
粗铜中所以的金属杂质,较铜活泼的金属失电子溶解,不活泼金属以单质形式沉积槽底;
由于有杂质金属失电子,导致两电极的质量变化值不相等。
本题难度:一般
4、选择题 1L某溶液中含有的离子如下表
| 离子 | Cu2+ | Al3+ | NO3- | Cl-
物质的量浓度(mol/L)
1
1
a
1
用惰性电极电解该溶液,当电路中有3mol e-通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是( )
A.电解后溶液呈酸性
B.a=3
C.阳极生成1.5mol Cl2
D.阴极析出的金属是铜与铝
参考答案:A.当电路中有3mole-通过时,阳极首先发生2Cl--2e
本题解析:
本题难度:一般
5、计算题 (8分)常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信 息(Ⅰ、Ⅱ两极分别代表两极各自产生的气体体积),通过计算推测: 息(Ⅰ、Ⅱ两极分别代表两极各自产生的气体体积),通过计算推测:
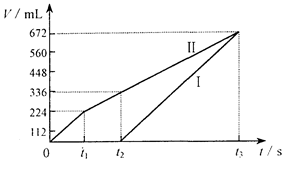
(1)原混合溶液NaCl和CuSO4的物质的量浓度。
(2)t2时所得溶液的pH。
参考答案: 本题解析:略 本题解析:略
本题难度:一般
|
|