微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知各物质的溶度积:
FeS:Ksp=6.3×10-18mol2?L-2
CuS:Ksp=1.3×10-36mol2?L-2
下列说法正确的是( )
A.同温度下,CuS的溶解度大于FeS的溶解度
B.同温度下,向饱和FeS溶液中加入少量Na2S固体后,Ksp(FeS)变小
C.向含有等物质的量的FeCl2和CuCl2的混合溶液中逐滴加入Na2S溶液,最先出现的沉淀是FeS
D.除去工业废水中的Cu2+,可以选用FeS做沉淀剂
参考答案:A、根据化学式相似的物质的溶度积常数越小,物质越难溶,溶解度
本题解析:
本题难度:简单
2、选择题 把氢氧化钙放入蒸馏水中,一定时间后达到如下平衡:Ca(OH)2(固)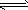 Ca2++2OH-加入以下物质,可使
Ca2++2OH-加入以下物质,可使
Ca(OH)2(固)减少的是[???? ]
A.NaCl
B.AlCl3溶液
C.NaOH
D.CaCl2
参考答案:B
本题解析:
本题难度:一般
3、选择题 已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16 ,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A.AgCl>AgI> Ag2CrO4
B.Ag2CrO4>AgCl>AgI
C.AgCl> Ag2CrO4>AgI
D.Ag2CrO4>AgI>AgCl
参考答案:B
本题解析:
试题分析:根据对应化学式相似的AgCl和AgI来说Ksp越小Ag+浓度越小,即AgCl>AgI;假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=2.0×10-12,x3=4.0×10-12,即X=
本题难度:一般
4、选择题 下列各项中的两个量,其比例为2:1的是(???)
A.pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH4+)与c(SO42-)之比
B.同温度下,0.2mol/LCH3COOH溶液与0.1mol/L CH3COOH溶液中的c(H+)之比
C.液面在“0”刻度,50mL酸式滴定管和25mL酸式滴定管内所盛溶液的体积
D.0.2mol/L的NaHSO3溶液中的阳离子与阴离子的浓度之比
参考答案:A
本题解析:略
本题难度:简单
5、实验题 (13分)工业上从废铅酸电池的铅膏回收铅的过程中,可用碳酸盐溶液与铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO32―(aq) PbCO3(s)+SO42―(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
PbCO3(s)+SO42―(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
(1)上述反应的平衡常数表达式:K=???????????????。
(2)室温时,向两份相同的样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化,在???????溶液中PbSO4转化率较大,理由是??????????????。
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3・Pb(OH)2],它和PbCO3受热都易分解生成PbO。该课题组对固体产物(不考虑PbSO4)的成分提出如下假设,请你完成假设二和假设三:
假设一:全部为PbCO3;
假设二:?????????????????;
假设三:?????????????????。
(4)为验证假设一是否成立,课题组进行如下研究。
①定性研究:请你完成下表中内容。
实验步骤(不要求写出具体操作过程)
| 预期的实验现象和结论
|
取一定量样品充分干燥,……
| ?
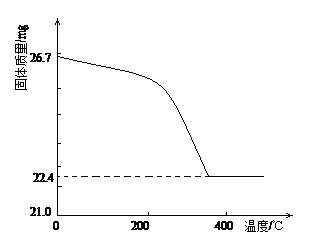
②定量研究:取26.7mg的干燥样品,加热,测的固体质量随温度的变化关系如下图。某同学由图中信息得出结论:假设一不成立。你是否同意该同学的结论,并简述理由:??????
?????????????????????????????????????????????????????????????。
参考答案:⑴K= c(SO42-)/c(CO32-)??
⑵ N
本题解析:⑴平衡常数表达式中的各物质的浓度为平衡浓度,且固体及纯液体的浓度为定值,不列在平衡常数表达式中,因此根据反应方程式容易写出反应的平衡常数表达式:K= c(SO42-)/c(CO32-)?。⑵HCO-3难电离,相同浓度时,Na2CO3溶液中CO2-3浓度远大于NaHCO3溶液中CO2-3的浓度,根据平衡移动原理CO2-3浓度大,平衡向正向移动,有利于PbSO4的转化。⑶根据信息及假设一,不难推出假设二和假设三分别为全部为PbCO3・Pb(OH)2、PbCO3与PbCO3・Pb(OH)2的混合物。⑷①若固体中
本题难度:一般
|