微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是( )
A.加入适量BaCl2(固体)?可以使溶液由d点变到c点
B.通过加水稀释可以使溶液由b点变到a点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp等于c点对应的Ksp
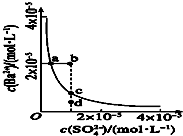
参考答案:A、硫酸钡溶液中存在着溶解平衡,c点在平衡曲线上,加入BaC
本题解析:
本题难度:简单
2、简答题 取一支洁净试管,向试管中加入0.1mol?L-1AgNO3溶液2mL,再向硝酸银溶液中加入稍过量的铜粉,反应足够长时间后,取上层清液于另一支试管中,再向该试管中滴加0.1mol?L-1KI溶液.回答有关上述实验的下列问题:
(1)可判断硝酸银溶液和铜的反应(正向反应)已确实发生的现象是______.
(2)可判断硝酸银溶液和铜的反应的逆反应也同时发生的现象是______.
(3)实验中若将KI溶液换成KCl溶液,则可能出现什么不同的现象?______.
参考答案:(1)Cu+2AgNO3=Cu(NO3)2+2Ag,AgNO
本题解析:
本题难度:一般
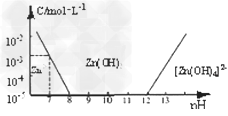
3、选择题 已知锌及其化合物的性质与铝及其化合物相似。如图,横坐标为溶液的pH,纵坐标为Zn2+离子或[Zn(OH)4]2-离子的物质的量浓度(假设Zn2+离子浓度为10-5mol・L-1时,Zn2+离子已沉淀完全)。下列说法不正确的是????
 [???? ]
[???? ]
A.往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为: Zn2++4OH-=[Zn(OH)4]2-
B.从图中数据计算可得Zn(OH)2的溶度积Ksp=10-17 mol3・L-3
C.某废液中含Zn2+离子,沉淀Zn2+离子可以控制溶液pH的范围是8~12
D.向1L1?mol・L-1 ZnCl2溶液中加入NaOH固体至pH=7,需NaOH?2mol
参考答案:D
本题解析:
本题难度:一般
4、选择题 一定温度下的难溶电解质AmBn在水溶液中达到溶解平衡时。已知下表数据
物质
| Fe(OH)2
| Cu(OH)2
| Fe(OH)3
|
Ksp/25℃
| 8.0×10-16
| 2.2×10-20
| 4.0×10-38
|
完全沉淀时的PH值
| ≥9.6
| ≥6.4
| 3~4
?
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是??
A.向该溶液中加少量铁粉不能观察到红色固体析出
B.该溶液中c(SO42-):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4
C.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
D.向该溶液中加入适量氯水,并调节pH值到3~4后过滤,得到纯净的CuSO4溶液
参考答案:D
本题解析:
试题分析:A.因为Fe3+的氧化性强于Cu2+,所以投入少量铁粉,先发生的反应是:2Fe3++Fe=3Fe2+,不能观察到红色固体析出,正确; B.因为Cu2+、Fe2+、Fe3+对应的碱全是弱碱,所以这三种离子在溶液中都会发生水解,因此它们的物质的量会减少,正确; C.从表格中可以看出,Fe(OH)3的Ksp是最小的,所以它最先出现沉淀,正确; D.加入氯水,可以把亚铁离子全氧化成三价,但它的还原产物Cl-肯定还在溶液中,而且在调节pH时加入的试剂也会在溶液中有所保留,所以得到的溶液中不可能只含
本题难度:一般
5、选择题 在Ca(OH)2(Ksp=5.5×10-6)、Mg(OH)2(Ksp=1.2×10-11)、AgCl(Ksp=1.56×10-10)三种物质中,下列说法正确的是
[ ??? ]
A.Mg(OH)2的溶解度最大
B.Ca(OH)2的溶解度最小
C.AgCl的溶解度最小
D.同条件下Ksp越大的溶解度也越大
参考答案:D
本题解析:
本题难度:一般
|