��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ʵ�������������ɫƿ�е�ҩƷ�ǣ�???��
A��Ũ����
B��Ũ����
C��Ũ����
D���Ȼ���
�ο��𰸣�A
���������
������������Ǽ����Էֽ���Լ�����Ҫ������ɫ�Լ�ƿ�У�Ũ��������ֽ⣬A��ȷ�������Լ�����Ҫ������ɫ�Լ�ƿ�У���ѡA��
�����������ǻ���������Ŀ��飬�ѶȲ�����Ҫ�ǿ���ѧ�����Լ����淽�����˽����ճ̶ȣ�����������ѧ�����ۺ�ʵ������������Ĺؼ���������ס������ѧ�Լ��ı��淽����ѧ�����ѵ÷֡�
�����Ѷȣ���
2��ѡ���� ���������У����Բ���������ʹ�õ���
A��©��
B����Ͳ
C����Һ��
D�����
�ο��𰸣�A
���������
���������������ʹ�õ������Dz��ܼ��ȵ�������©���ɳ��ȹ��ˣ���Ͳ����Һ�ܡ��ζ��ܶ����ܼ���ʹ�ã����Դ�ѡA��
�����Ѷȣ���
3��ʵ���� ����������һ�r������ʳƷ���Ӽ���ʹ��ʱ�����ϸ������������Ϊ���ijʳƷ���������κ�����ͨ����1kg��Ʒ�к�NaNO2��������)��ij�о�С���������������ʵ�鷽����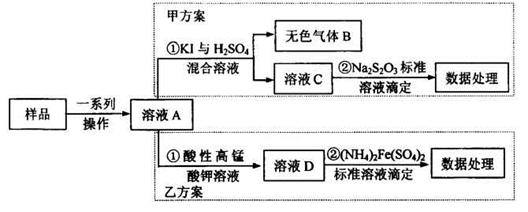
(1)��ɫ����B�������Ժ���ɫ��B�Ļ�ѧʽΪ_______д���������з�Ӧ�����ӷ���ʽ_______
(2)��ɲ���ƽ�ҷ������з�Ӧ�����ӷ���ʽ
MnO4-+??NO2-+?????????=???Mn2++???NO3-+?????????,
(3)�ҷ�������������100mL0.0010mol/L(NH4)2Fe(SO4)2����Һ������ȷ������Ʒ����������Ҫ�������У���Ͳ���ձ���_______������Һʱ�����ݵIJ���������______
(4)��ȡ��Ʒag�����ҷ������вⶨ��ȷ��ȡ12.00mL0.0005mol/L�����Ը��������Һ����ͯ������ҺA��Ӧ����Ӧ����Һ��0.0010mol/L(NH4)2Fe(SO4)2����Һ�ζ�����ɫ��Һ�պ���ȥ���ظ�����ʵ��2�Σ�ƽ������(NH4)2Fe(SO4)2��Һ10.00mL.��1kg��Ʒ��NaNO2������Ϊ_______mg.
�ο��𰸣���14�֣�
��1��NO?��1�֣���? 2I�� +2NO
���������
����������������̵Ľ���Ĺؼ��������������ʲô���ʣ�����ʲô��Ӧ��������ԭ��Ӧ�Ӷࣩ����η���ȡ��������ҷֱ�Ϊ������ԭ��Ӧ�������õ���������������ԣ��������õ���������Ļ�ԭ�ԣ�������ʽ�ֱ�Ϊ���ף�2I�� +2NO2��+4H+ =I2+ 2NO��+2H2O���ң�2MnO4��+ 5NO2��+ 6 H+? =" 2" Mn2+? + 5NO3��+ 3H2O��Ȼ�����Na2S2O3�ζ�I2������(NH4)2Fe(SO4)2�ζ�����������أ����ݵζ��������Լ��㡣��4��5Fe2+~MnO4-��n(MnO4-)=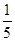 ��0.0010��0.01=2��10-6mol���ҷ��������ĵĸ������Ϊ0.012L��0.0005mol/L-2��10-6mol=4��10-6mol��n��NaNO2��=
��0.0010��0.01=2��10-6mol���ҷ��������ĵĸ������Ϊ0.012L��0.0005mol/L-2��10-6mol=4��10-6mol��n��NaNO2��=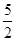 ��4��10-6mol=10-5mol����ÿkg�к���690/amg��
��4��10-6mol=10-5mol����ÿkg�к���690/amg��
�����Ѷȣ�һ��
4��ѡ���� ����������װ����ʹ��ǰһ��Ҫ��������Ե��ǣ�������
A������ƿ
B��ϴ��ƿ
C����Һ©��
D���ᣨ�ʽ�ζ���
�ο��𰸣�B
�����������
�����Ѷȣ���
5��ѡ���� ���������ɼ��ȵ���
A��Բ����ƿ
B����Һ©��
C������ƿ
D��ϸ��ƿ
�ο��𰸣�A
������������Լ��ȵ�����ΪԲ����ƿ����Һ©����Զ��Һ������ȡ������ƿ���ݣ�ϸ��ƿװҺ̬�����ʡ�
�����Ѷȣ���