微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 工业制硫酸时,利用催化氧化反应将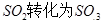 是一个关键的步骤。
是一个关键的步骤。
(1)某温度下,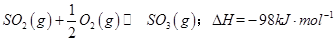 。开始时在100L的密闭容器中加入4.0molSO2(g)和10.0molO2,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=____________。
。开始时在100L的密闭容器中加入4.0molSO2(g)和10.0molO2,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=____________。
(2)一定条件下,向一带活塞的密闭容器中充入2mol mol
mol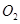 ,发生反应:
,发生反应: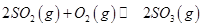 ,达平衡后改变下述条件,
,达平衡后改变下述条件,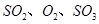 气体平衡浓度都比原来增大的是____________(填字母)。
气体平衡浓度都比原来增大的是____________(填字母)。
A.保持温度和容器体积不变,充入2mol
B.保持温度和容器体积不变,充入2molN2
C.保持温度和容器内压强不变,充入1mol
D.移动活塞压缩气体
E.升高温度
(3)下列关于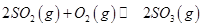 反应的图像中,不正确的是_________。
反应的图像中,不正确的是_________。
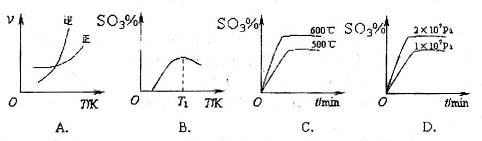
(4)同学们学习了电化学知识后大家提出,可以用电解的方法来生产硫酸,可避免产生酸雨,污染环境。于是大家设计了一个以铂为电极,两极分别通入SO2和空气,酸性电解液来实现电解生产硫酸。
①阳极的电极反应为______________________________。
②若电解液为2L0.025mol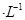 的硫酸溶液,当电解过程共转移了0.1mol电子时,理论上消耗SO2的体积为(标准状况)为_________,此溶液的pH="__________" (忽略溶液体积变化)。
的硫酸溶液,当电解过程共转移了0.1mol电子时,理论上消耗SO2的体积为(标准状况)为_________,此溶液的pH="__________" (忽略溶液体积变化)。
③设计此实验的想法得到了老师的充分肯定,但与工业上生产硫酸相比还是有很多不足,请对此实验进行合理的评价____________________________(写出一点即可)。
2、选择题 在一定温度下,向容积固定不变的密闭容器中充入amolNO2,发生如下反应:
2NO2(g) N2O4(g);△H<0。达平衡后再向容器中充入amolNO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是(???? )
N2O4(g);△H<0。达平衡后再向容器中充入amolNO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是(???? )
A.平均相对分子质量增大
B.NO2的转化率提高
C.NO2的质量分数增大
D.反应放出的总热量大于原来的2倍
3、选择题 某温度下,反应2A(g) B(g)(正反应为吸热反应)在密闭容器中达到平衡,平衡后
B(g)(正反应为吸热反应)在密闭容器中达到平衡,平衡后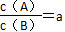 ,若改变某一条件,足够时间后反应再次达到平衡状态,此时
,若改变某一条件,足够时间后反应再次达到平衡状态,此时 ,下列叙述正确的是? ( )。
,下列叙述正确的是? ( )。
A.在该温度下,保持容积固定不变,向容器内补充了B气体,则a<b
B.若a=b,则B容器中一定使用了催化剂
C.若其他条件不变,升高温度,则有a<b
D.若保持温度、压强不变,充入惰性气体,则有a>b
4、计算题 (7分)某固定容积的2L密闭容器中进行反应 :?起始时加入的N2、H2、NH3均为2mol,5min后反应达到平衡, NH3的物质的量为3mol,求:
:?起始时加入的N2、H2、NH3均为2mol,5min后反应达到平衡, NH3的物质的量为3mol,求:
(1)这5分钟内用N2来表示该反应的反应速率(请写出计算过程,下同)
(2)求平衡时H2的物质的量浓度
(3)平衡时容器的压强为初始时的几分之几?
5、选择题 在一定温度下,将等物质的量A和B充入一密闭容器中,发生如下反应:A(g)+2B(g)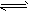 2C(g),反应达到平衡时,若A和B的物质的量之和与C相等,则此时A的转化率为[???? ]
2C(g),反应达到平衡时,若A和B的物质的量之和与C相等,则此时A的转化率为[???? ]
A.50%
B.60%
C.40%
D.70%