微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述中,不正确的是
A.在相同条件下,焓变小于0而熵变大于0的反应肯定能自发进行
B.升高温度会加快化学反应速率,其原因是增加了活化分子的百分数
C.沉淀转换的实质就是沉淀溶解平衡的移动,平衡一般向生成更难溶物质的方向移动
D.PH为10的氨水,由水电离出的氢氧根离子浓度为10-4 mol/L
参考答案:D
本题解析:略
本题难度:一般
2、选择题 25℃和1.01×105 Pa时,反应2N2O5(g)=== 4NO2(g)+O2(g) ΔH=+56.76kJ/mol,自发进行的原因是
A.是吸热反应
B.是熵减反应
C.熵增效应大于能量效应
D.熵增效应小于能量效应
参考答案:C
本题解析:
试题分析:反应是焓增的熵增的反应,熵增效应大于能量效应,才会使复合判据小于0,反应自发进行,所以选C。
考点:化学反应进行的方向。
本题难度:一般
3、填空题 有可逆反应A(g)+B(g)  2C(g),在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。填写下列空白:
2C(g),在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。填写下列空白:
⑴反应在????????????温度下达到平衡。???⑵正反应为??????????热反应(填“放”或“吸”)。??????⑶由T3向T4变化时,v正????????v逆(填“>”、“<”或“=”)。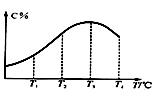
参考答案:⑴ 本题解析:略
本题解析:略
本题难度:简单
4、选择题 下列说法不正确的是
A.反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H<0
B.常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小
C.铅蓄电池在放电过程中,正、负极质量都减小
D.温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变
参考答案:C
本题解析:A中反应是熵值减小的反应,根据△G=△H-T・△S可知,反应能够自发进行,则反应一定是放热反应,A正确。加入少量NH4Cl晶体,则c(NH4+)增大,从而抑制氨水的电离,所以碱性降低,pH减小,B正确。铅蓄电池在放电过程中,正、负极均生成硫酸铅,电极质量增大,所以选项C不正确。水的离子积常数Kw只与温度有关系,所以选项D是正确的,答案选C。
本题难度:一般
5、填空题 在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通(如上图)。

容器中发生以下反应:N2+3H2 2NH3(正反应放热),若反应达到平衡后,测得混合气体为7体积。据此回答下列问题:
2NH3(正反应放热),若反应达到平衡后,测得混合气体为7体积。据此回答下列问题:
(1)保持上述温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各物质的体积分数仍与上述平衡时完全相同。那么:①若a=1,c=2,则b=_________,在此情况下,反应起始时将向_____________(填“正”或“逆”)方向进行。
②若需规定起始时,反应向逆方向进行,则c的范围是___________。
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是_________,原因是______________________________。
参考答案:
 本题解析:略
本题解析:略
本题难度:简单