微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是(??)
A.1 mol H2O的质量是18 g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量是32 g
D.标准状况下,1 mol任何物质体积均为22.4 L
参考答案:C
本题解析:质量的单位是g,而摩尔质量的单位是g/mol,所以选项A和B都是错误的;3.01×1023个SO2分子的物质的量是3.01×1023÷6.02×1023/mol=0.5mol,则SO2的质量是0.5mol×64g/mol=32g,选项C正确;标准状况下,1 mol任何气体物质体积均为22.4 L,选项D不正确,答案选C。
本题难度:一般
2、选择题 向MgCl2、AlCl3的混合溶液开始滴加6mol/L的试剂A,之后改滴试剂B,所得沉淀物质的量Y(mol)与试剂体积V(mL)间的关系如图所示。以下结论不正确的是(?)
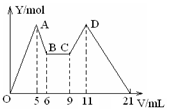
A.从6到9,相应离子反应方程式为H++OH-=H2O
B.A 是NaOH,B是盐酸,且c(NaOH):c( HCl) = 2:1
C.原混合液中,c(Al3+):c(Mg2+):c(Cl-) = 1:1:5
D.A是盐酸,B是NaOH, 且c(NaOH) =" 2c" (HCl)
参考答案:D
本题解析:
试题分析:由6mL和9mL对应液体中沉淀量相等,可以推知此时仅仅发生酸碱中和反应,即H++OH-=H2O,故A正确;由图可知,5→6(1 mL)、9→11(2 mL)分别是溶解Al(OH)3和使AlO2-恰好完全生成Al(OH)3沉淀消耗的NaOH和HCl.根据铝元素守恒:
NaOH-Al(OH)3-AlO2--H+
1???? 1??????? 1???? 1
由此可以推出:c(NaOH):c(HCl)=2:1,故B正确;从加入5 mL A生成沉淀最多,再继续加1 mL A沉淀
本题难度:一般
3、填空题 (10分)A、B、C、 D四种溶液分别是NaOH溶液、氨水、 CH3COOH溶液、盐酸中的一种。常温下:
①浓度均为0.1mol・L-1的A和C溶液,pH:A<C<7;
②将1 L pH=3的A溶液分别与0.001mol・L-1?xL B溶液、0.001mol・L-1??yL D溶液充分反应至中性,x、y大小关系为: y<x;
回答下列问题:
(1)D是??????????????????????(填化学式)溶液;??????????????????????????????????????????????????????
(2)②中1LpH=3的A溶液与0.001mol・L-1 xL B溶液充分反应至中性,所 得溶液中各种离子的物质的量浓度由大到小的顺序为??????????????????????????????????。
得溶液中各种离子的物质的量浓度由大到小的顺序为??????????????????????????????????。
(3)常温下,等体积且等物质的量浓度的C溶液和D溶液充分混合后所得溶液的pH
???????7(填“>”、“<”或“=”),用离子方程式解释其原因????????????????。
(4)向pH相同且等体积的两份溶液A和C中,分别投入质量不同的锌粉反应,若放出氢气的质量相同,则下列说法正确的是??????????????????(填写序号)。
①开始反应时的速率A>C????????????????②反应所需要的时间C>A?
③参加反应的锌粉物质的量A="C??????????" ④A溶液里有锌粉剩余
参考答案:(1)NaOH (2分)??????????????????
本题解析:略
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数的值。下列判断正确的是
A.64g O3含有的分子数目为2NA
B.标准状况下,22.4 L H2O含有的氢原子数目为2NA
C.1 L 1mol・L-1 CaCl2溶液中含有的氯离子数目为2NA
D.56g铁在足量氯气中完全燃烧转移的电子数目为2NA
参考答案:C
本题解析:
试题分析:A.64g O3含有的分子数目为(64/48)×NA=4/3NA,错误;B.标准状况下,H2O是液体,无法计算物质的量,错误;C.1 L 1mol・L-1 CaCl2溶液中含有的氯离子数目为2NA,正确;D.铁与氯气反应生成高价氯化物,56g铁在足量氯气中完全燃烧转移的电子数目为3NA,错误;选C。
考点:考查阿伏伽德罗常数及计算。
本题难度:一般
5、选择题 下列说法一定正确的是
A.0.5 mol Cl2所占体积约为11.2 L
B.16 g O2中含有的分子数约为6.02×1023
C.0.1 mol/L NaCl溶液中含溶质的物质的量为0.1 mol
D.标准状况下,11.2 L N2和CO的混合气体所含原子数约为6.02×1023
参考答案:D
本题解析:
试题分析:A为指明所处的条件为标准状况,故气体的摩尔体积不一定为22.4L/mol,A错误;16g氧气的物质的量为16g/32g/mol=0.5mol,分子数为3.01×1023,,B错误;C未指明溶液的体积,C错误;11.2 L 气体的物质的量为 =0.5mol,二者均为双原子分子,所含原子数为0.5molx2x6.02×1023mol-1,D正确,答案选D.
=0.5mol,二者均为双原子分子,所含原子数为0.5molx2x6.02×1023mol-1,D正确,答案选D.
考点:气体的摩尔体积
本题难度:一般