微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设阿伏加德罗常数的值为NA,下列说法正确的是( )
A.标准状况下,22.4 L一氯甲烷和二氯甲烷的混合物所含氯原子数介于NA至2NA之间。
B.1 mol的Cu在一定条件下与足量硫粉反应,转移电子数目为2NA
C.3.65 g液态氯化氢中分子的数目为0.1NA
D.常温下5.6 g铁投入足量的浓硝酸中,转移的电子数为0.3NA
参考答案:C
本题解析:二氯甲烷标准状况下为液态,A项错误;Cu与S反应,2Cu+S Cu2S,产物中Cu的化合价为+1价,故1 mol Cu反应,转移的电子数目为NA,B项错误;3.65 g液态HCl即为0.1 mol,含有的分子数目为0.1NA,C项正确;常温下Fe在浓HNO3中钝化,D项错误。
Cu2S,产物中Cu的化合价为+1价,故1 mol Cu反应,转移的电子数目为NA,B项错误;3.65 g液态HCl即为0.1 mol,含有的分子数目为0.1NA,C项正确;常温下Fe在浓HNO3中钝化,D项错误。
本题难度:一般
2、选择题 已知:一般溶液浓度越大密度越大,氨水等例外。则体积为vL、质量为mg,浓度为a mol/L的氨水溶液的溶质质量分数为b%,用水稀释到0.5a mol/L,下列说法正确的是
A.加水的体积为vL
B.加水的质量为mg
C.0.5amol/L的氨水质量分数等于0.5b%
D.0.5amol/L的氨水质量分数小于0.5b%
参考答案:D
本题解析:
试题分析:A、氨水溶液的浓度越大,密度越小。加入等体积的水,溶液的质量分数小于0.5b%,但氨水溶液的密度增大,所以根据c= 可知,此时溶液的浓度不一定是0.5amol/L,A错误;B、如果加入等质量的水,则溶液的质量分数等于0.5b%,但氨水溶液的密度增大,所以根据c=
可知,此时溶液的浓度不一定是0.5amol/L,A错误;B、如果加入等质量的水,则溶液的质量分数等于0.5b%,但氨水溶液的密度增大,所以根据c= 可知,此时溶液的浓度大于0.5amol/L,B错误;C、0.5amol/L的氨水溶液的密度大于浓度为a mol/L的氨水溶液的密度,因此根据c=
可知,此时溶液的浓度大于0.5amol/L,B错误;C、0.5amol/L的氨水溶液的密度大于浓度为a mol/L的氨水溶液的密度,因此根据c= 可知,0.5amol/L的氨水溶液的质量分数小于0.5b%,C错误;D、根据C中分析可知0.5amol/L的氨水溶液的质量分数小于0.5b%,D正确,答案选D。
可知,0.5amol/L的氨水溶液的质量分数小于0.5b%,C错误;D、根据C中分析可知0.5amol/L的氨水溶液的质量分数小于0.5b%,D正确,答案选D。
考点:考查物质的量浓度与质量分数的有关计算
本题难度:一般
3、选择题 下列叙述正确的是
A.48gO3气体含有6. 02×1023个O3分子
02×1023个O3分子
B.常温常压下,4.6gNO2气体含有1.81×1023个NO2分子
C.0.5mol・ L-1CuCl2溶液中含有3.01×1023个Cu2+
L-1CuCl2溶液中含有3.01×1023个Cu2+
D.标准状况下,33.6LH2O含有9.03×1023个H2O分子
参考答案:A
本题解析:解题时要注意回忆概念、分析原理注意运算公式的适用范围。B选项4.6gNO2气体中理论上含有1mol NO2分子,约6.02×1023个NO2分子,由于2NO2 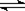 N2O4,故应小于6.02×1
N2O4,故应小于6.02×1 本题难度:简单
本题难度:简单
4、选择题 某金属氯化物的溶液20mL,物质的量浓度为0.05mol/L,恰好与20mL 0.15mol/L的AgNO3溶液完全反应,则该氯化物的化学式为 ( )
A.RCl
B.RCl2
C.RCl3
D.RCl4
参考答案:C
本题解析:
试题分析:RCln的物质的量是20mL*0.05(mol/L)/1000(mL/L)=0.001mol
AgNO3的物质的量是20mL*0.15(mol/L)/1000(mL/L)=0.003mol
假设金属氯化物的化学式为RCln,则发生反应的方程式为:
RCln+ nAgNO3 = R(NO3)n + nAgCl↓
1 n
0.001mol 0.003mol
1*0.003mol=0.001n
解得n=3。
故金属氯化物的化学式为RCl3。
故选C。
考点:物质的量浓度的计算
点评:本题考查的是化学计量在化学方程式中的计算,题目难度不大,注意物质的量与物质的量浓度之间的计算关系。
本题难度:一般
5、选择题 现有三种常见治疗胃病药品的标签:

① ② ③
药品中所含的物质均能中和胃里过量的盐酸,下列关于三种药片中和胃酸的能力比较,正确的是
A.①=②=③
B.①>②>③
C.③>②>①
D.②>③>①
参考答案:C
本题解析:
试题分析:三种常见治疗胃病的药治疗过程为:
CaCO?+ 2HCl = CaCl?+ H?O + CO?↑
Mg(OH)2+2HCl=MgCl2+2H2O
MgO+2HCl==MgCl2+H2O
CaCO?的摩尔质量是100g/mol ;Mg(OH)2的摩尔质量是58g/mol;MgO的摩尔质量是40g/mol;
相同物质的量的CaCO?;Mg(OH)2;MgO消耗相同物质的量的盐酸,而每片药的质量都相同,所以相同质量的药片,三种药的物质的量的关系是:③>②>①所以,三种药片中和胃酸的能力比较是:③>②>① 。故选C。
考点:化学计算
点评:相同质量的物质,摩尔质量越大,其物质的量越小。本题考查常用化学计量计算、根据方程式的计算,比较基础,注意基础知识的掌握。
本题难度:简单