��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵����ȷ����
A��������ԭ��Ӧ�ı�����Ԫ�ػ��ϼ۷����仯
B����ԭ����һ���ܹ��õ����ӵ�����
C����������Ԫ�ػ��ϼ����ߵķ�Ӧ�ǻ�ԭ��Ӧ
D��������Ӧ�ͻ�ԭ��Ӧ��ͬʱ������
�ο��𰸣�D
�������������һ�����Ŀ��飬������ԭ��Ӧ�ı�����Ԫ��ԭ�Ӽ�ĵ��ӵ�ʧ��ƫ�룻��ԭ�����ڻ�ѧ��Ӧ��ʧȥ�˵��ӵ����ʣ���������Ԫ�ػ��ϼ����ߵķ�Ӧ��������Ӧ��
�����Ѷȣ���
2������� ��14�֣���1��һ������50 kg�Ľ����������к���2 g�����������в���������̬����ʽ���ڣ�������Fe2+��Fe3+��ʽ���ڡ�Fe2+�ױ����գ���ƶѪ�߲�����ʱ��Ӧ���躬Fe2+���Σ�������������FeSO4��������ά����C����ʹʳ���е�Fe3+ת��ΪFe2+��������������,�ù�����ά����C��??????����Fe3+��??????����ά����C�Ļ�ԭ��______�� Fe2+���ǿ����������
��2�����ȵ�ϡ������Һ���ܽ���11.4 g FeSO4��������50 mL 0.5 mol/L KNO3��Һ��ʹ���е�Fe2+ȫ��ת����Fe3+��KNO3Ҳ��Ӧ��ȫ������NxOy�������������ݳ���
____FeSO4 + ???KNO3 + ???H2SO4 =??K2SO4 + ???Fe2��SO4��3 + ???NxOy + ???H2O
����ƽ�û�ѧ����ʽ���õ����ű������ת�Ƶķ������Ŀ��
�ڷ�Ӧ��������Ϊ???????????????����������Ļ�ѧʽΪ__________
��3���ǰ���NH2OH����һ�ֻ�ԭ������25��00 mL 0��049 mol/L�ǰ���������Һ����������������Һ����������·�Ӧ�����ɵ�Fe2+����ǡ����24��5 mL 0��020 mol/L��KMnO4������Һ��Ӧ������������Ӧ�У� Fe2+���������Ը�����ط�Ӧ�����ӷ���ʽΪ��________________________���ǰ�������������??????????????????????��
�ο��𰸣�(1)��ԭ?����?ǿ��ÿ��1�֣�
(2)��6FeSO4
�����������1������ά����C����ʹʳ���е�Fe3+ת��ΪFe2+��˵��ά���أþ��л�ԭ�ԣ���������������������������ԭ��Ӧ�У���������������ǿ����������ģ���ԭ���Ļ�ԭ��ǿ�ڻ�ԭ����ģ�����ά���أõĻ�ԭ��ǿ���������ӵġ�
��2��11.4 g FeSO4��0.075mol����Ӧ��ʧȥ0.075mol��50 mL 0.5 mol/L KNO3��0.025mol�����Ը��ݵ��ӵĵ�ʧ�غ��֪��1mol����صõ�3mol���ӡ���˵�ԭ�ӵĻ��ϼ۴ӣ�5�۽��͵���2�ۣ���ԭ������NO�����ݵ��ӵĵ�ʧ�غ��ԭ���غ����ƽ
�����Ѷȣ�һ��
3������� ��9�֣��������ƣ�NaClO2����һ����Ҫ�ĺ�������������Ҫ����ˮ�������Լ�ɰ�ǵ�Ư����ɱ�����������ù������ⷨ�����������ƵĹ�������ͼ��
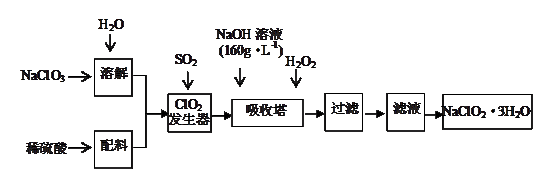
��֪��NaOH��Һ��160g��L-1����ָÿ����Һ�к�����160 g��
�Իش��������⣺
��1����NaOH��Һ�����ʵ���Ũ��Ϊ???????????��
��2�����������У�ClO2��NaOH��H2O2��Ӧ����NaClO2��O2����÷�Ӧ�л�ԭ���������������ʵ���֮��Ϊ?????????��
��3��NaClO2���ȶ�����������ڼ���ʱ���û�ʱ������������ը���䱬ը��IJ��������
?????????������ĸ��
A��NaCl��Cl2
B��NaCl��NaClO
C��NaClO3��NaClO4
D��NaCl��NaClO3
(4)NaClO3��SO2��Ӧ����ClO2��д���÷�Ӧ�Ļ�ѧ����ʽ�����õ����ű������ת�Ƶķ������Ŀ��?????????????????????????????????????????????????????????????????��
�ο��𰸣���1��4mol/L ------2��??��2��1:2----
�����������1��NaOH��Һ��160g��L-1���������ʵ���Ũ����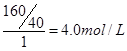 ��
��
��2����Ԫ�صĻ��ϼ۴ӣ�4�۽��͵���3�ۣ���Ԫ�صĻ��ϼ۴ӣ�1�����ߵ�0�ۣ�����������ClO2�ͻ�ԭ��H2O2�����ʵ���֮����2�U1��
��3�����������֪����Ԫ�صĻ��ϼۼ����ߣ������ͣ�����ѡ��D��ȷ��
��4����Ԫ�صĻ��ϼ۴ӣ�5�۽�
�����Ѷȣ�һ��
4��ѡ���� ��NaIO3�ļ�����Һ��ͨ�����������Եõ�Na2H3IO6�������йظ÷�Ӧ��˵���������
A���ڸ÷�Ӧ��NaIO3����ԭ��
B�����������£�����������ǿ��Na2H3IO6
C����Ӧ������1mol Na2H3IO6��ת��2mol����
D����Ӧ�����������뻹ԭ��������ʵ�����Ϊ2:1
�ο��𰸣�D
���������
��������� IO3����Cl2��3OH��=H3IO62����2Cl����A����Ӧ��NaIO3����ԭ������ȷ��B��ͬһ������ԭ��Ӧ����������������ǿ����������������ԣ���ȷ�� C����Ӧ������1mol Na2H3IO6��ת��2mol���ӣ���ȷ��D����Ӧ�����������뻹ԭ��������ʵ�����Ϊ1:2������
�����Ѷȣ�һ��
5������� ��6�֣�ʵ����Ҳ����KMnO4�����Ũ���ᷴӦ����������Ӧ����ʽ���£�
2KMnO4��16HCl(Ũ)��2KCl��2MnCl2��8H2O��5Cl2��
����������⣺
��1���÷�Ӧ����������????����ԭ����?????������������?????����ԭ������??????��
��2����˫���ű���÷�Ӧ�ĵ��ӵ�ʧ�ķ������Ŀ??????????????????????????��
�ο��𰸣�(1)KMnO4��HCl��Cl2��MnCl2���������֣�����
�����������1��������Ϊ����Ԫ�ػ��ϼ۽��͵����ʣ���Ӧ�����ɻ�ԭ�����ԭ��Ϊ����Ԫ�ػ��ϼ����ߵ����ʣ���Ӧ�������������
��2��
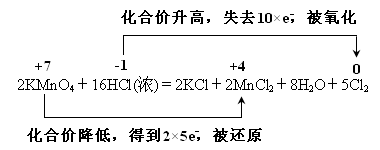
�����Ѷȣ�һ��