��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��NH4��2SO4��ǿ�������·����ֽ⣬����NH3��SO2��N2��H2O���÷�Ӧ������������������ͻ�ԭ��������ʵ���֮���ǣ�???��
A��1��3
B��3��1
C��3��4
D��4��3
�ο��𰸣�A
���������N2���������SO2�ǻ�ԭ������
 ʧȥ����3e-��2=6e-
ʧȥ����3e-��2=6e-
 �õ�����2e-��3=6e-
�õ�����2e-��3=6e-
��
�����Ѷȣ���
2������� ��7�֣�����֪��CuI��������ˮ�İ�ɫ���塣������Cu2+>I2> Cu+����ԭ��Cu>I-> Cu+
��1���������������Ի�ԭ�Ե�ǿ���Ʋ⣬����Һ��Cu2+��I����Ӧ�IJ�����??????��??????��
��2�������ڿ����е�HI��Һ�ʻ�ɫ�������м���һЩͭ�ۣ���ʹ��Һ��ɫ��ʧ����Ӧ�Ļ�ѧ����ʽΪ_______________________��
��3����������2����HI��Һ�Ļ�ɫ��Ҳ��������ͨ������H2S��������Ϊ��Ũ�Ƚӽ�ʱ����ԭ��H2S_______���>������<������=����I���������ͭ�۵ķ�����ȣ��ô˷����õ���HI��ҺŨ��________����ߡ������͡�������ȡ�����
��4��CuI�����ڼ��������Ƿ��й�������4CuI(��ɫ)��Hg��Cu2HgI4(����ɫ)��2Cu�����й��ڸû�ѧ����ʽ��˵���������_____________��
a��?�÷�Ӧ��������Ԫ����ͭԪ�غ�Ԫ��
b���÷�Ӧ��������ΪCuI
c��Cu2HgI4���������������ǻ�ԭ����????????
�ο��𰸣���7�֣���1��CuI��I2��2�֣�????��2��2Cu��I2
���������
�����������1��������Cu2+>I2> Cu+����ԭ��Cu>I-> Cu+����������Һ��Cu2+��I����Ӧ�IJ���Ӧ����CuI��I2��
��2�������ڿ����е�HI��Һ�ʻ�ɫ��˵���е��ʵ����ɣ����Լ���ͭ��ķ�Ӧ����ʽ��2Cu��I2 =2CuI����
��3������Ļ�ԭ�Դ��ڵ����ӵģ�����Ҳ����ͨ�����ԭ�ⵥ�ʡ������ڸ÷�Ӧ�еⵥ��ȫ������ԭ���ɵ⻯�⣬����Ũ�ȸߡ�
��4�����ݷ�Ӧ�ķ���ʽ��֪��Hg�Ļ��ϼ����ߣ�����ԭ����ͭԪ�صĻ��ϼ۴ӣ�1�۽��͵�0�ۣ�����
�����Ѷȣ�һ��
3��ѡ���� п�����ϡ���������������п������狀�ˮ������һ������ԭ��Ӧ�У���������1 mol Zn�����HNO3�����ʵ���Ϊ��???��
A��2.5 mol
B��4 mol
C��0.25 mol
D��0.5 mol
�ο��𰸣�A
�����������������ƽ����ʽΪ��4Zn+10HNO3====4Zn(NO3)2+NH4NO3+3H2O
�����Ѷȣ���
4��ѡ���� ���Ϸ�Ӧ���ֽⷴӦ���û���Ӧ���ֽⷴӦ �����ֻ�����ѧ��Ӧ���͡����б仯����������ԭ��Ӧ�����Dz��������ֻ�����Ӧ���͵���?
[?????]
A��CO+ CuO Cu+ CO2
Cu+ CO2
B��2Al + Fe2O3 Al2O3+ 2Fe
Al2O3+ 2Fe
C��2O3 3O2
3O2
D��Cl2+ 2FeCl2==2FeCl3
�ο��𰸣�A
���������
�����Ѷȣ���
5������� ������ԭ��Ӧ�������������о��й㷺����;���ᴩ�Ž�
��1����������������������з�����������ԭ��Ӧ����??????��
��2��ˮ���������Ҫ��ɲ��֣��������к�������һ�����ʡ��������ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��Ҳ������ͼ���
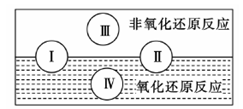
��д����ˮ�μӡ�ˮΪ��ԭ����Ϊ���͢���һ����ѧ����ʽ��????????????????????????????��
��3��NaNO2��һ��ʳƷ���Ӽ��������°�������KMnO4��Һ��NaNO2��Ӧ�����ӷ���ʽ�ǣ�

���벹����������ƽ����ʽ���������ת�Ƶķ������Ŀ��
��ijͬѧ��ȡ��7.9 g KMnO4�����壬������100 mL��Һ���ش��������⣺
��ʵ���У�ʹ������ƿʱҪ����Ƿ�©ˮ���������???????????????????????????��
�۲��淶��ʵ������ᵼ��ʵ�����������в�����ʹʵ����ƫС����??????(�����)��
A�����ܽ������������Һ�彦���ձ���
B������ʱ��������ƿ�ϵĿ̶���
C�����ݺ�����ƿ��ҡ�Ⱥ��÷���Һ����ڿ̶��ߣ������ּ�������ˮ���̶���
��ijͬѧ��������õ�KMnO4��Һ�ζ�δ֪Ũ�ȵ�NaNO2��Һ��ȡ20 mLδ֪Ũ�ȵ�NaNO2��Һ����ƿ��ȡ������õ�KMnO4��Һ��________(���ʽ����ʽ��)�ζ��ܣ��ζ���ɺ�����KMnO4��Һ10 mL����NaNO2��Һ��Ũ��Ϊ________________��
�ο��𰸣���1��D????��2�� 2F2 + 2H2O =" 4HF"
���������
�����������1��A��B��C���������仯��Dȼ���ǻ�ѧ��Ӧ���Ҷ�����������ԭ��Ӧ����2�����ֻ�����Ӧ����?������������ԭ��Ӧ��ֻ���û���Ӧ��ˮ����ԭ������ֻ����Ԫ�ر���������ϵ������ˮ�ķ�Ӧ��д����ѧ����ʽ��2F2 + 2H2O =" 4HF" + O2����3���ٷ�Ӧ��������Һ�н��У����Է�����Ӧ��дH+��Mn�Ļ��ϼ۽���5(+7��+2)��NԪ�صĻ��ϼ�����2(+3��+5)������MnO4�C��Mn2+����2��NO2�C��NO3�C����5�����ݵ���غ㣬H+��6������ԭ�Ӹ����غ�H2O��3���ڼ������ƿ�Ƿ�
�����Ѷȣ�һ��