微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据元素周期律和化学键的相关知识,分析下面的推断中错误的是(???)
A.Al原子失电子能力比镁弱
B.HNO3酸性比H2CO3强
C.NaOH碱性比Mg(OH)2强
D.HCl能电离产生H+和Cl―,所以HCl是离子化合物
2、填空题 (10分)A、B、C、D、E、F、G、H、IJ分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),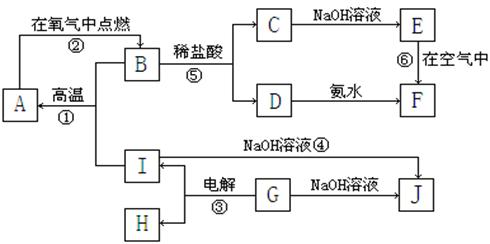
且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第_______周期、第_______族;
(2)写出反应①的化学方程式___________????????????????????????????_________;
(3)写出反应④的离子方程式_____________????????????????????????????_______;
(4)写出反应③的电极方程式:
阳极:_______________??_____??????阴极:____________?????__________
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是___________。(填序号)
3、选择题 下列叙述不正确的是????????????????????????????????????????????(???)
A.H2S、H2O、HF的稳定性依次增强
B.RbOH、KOH、Mg(OH)2的碱性依次减弱
C.Na+、Mg2+、Al3+的氧化性依次减弱
D.H4SiO4、H2CO3、H2SO4酸性依次增强
4、选择题 试判断116号新元素在周期表中的位置
A.第6周期ⅣA族
B.第7周期ⅥA族
C.第7周期Ⅷ族
D.第8周期ⅥA族
5、推断题 (1)1807年,英国化学家戴维在研究中发现:电解条件下可把水分解成H2和O2。他设想用电解的方法从KOH、NaOH中分离出K和Na。最初,戴维用饱和KOH溶液进行电解,不料还是得到H2和O2。这时,他考虑在无水条件下继续这项实验,但是,实验中产生的金属液珠一接触空气就立即燃烧起来;这时,他又考虑在________条件下电解熔融的KOH继续实验,最后他终于成功地得到了银白色的金属钾。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,质量数是85。根据材料回答下列问题:
Ⅰ.铷位于元素周期表的第________周期________族。
Ⅱ.关于铷的下列说法中正确的是________(填序号,下同)。
①与水反应比钠更剧烈?②Rb2O在空气中易吸收水和二氧化碳?③Rb2O2与水能剧烈反应并释放出O2?④它是极强的还原剂?⑤RbOH的碱性比同浓度的NaOH弱
Ⅲ.现有铷和另一种碱金属形成的合金5? g,与足量水反应时生成标准状况下的气体2.24? L,则另一碱金属可能是________(填元素符号)。