微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 A、B、C、E、F为原子序数依次增大的六种元素,其中A、B、C、D、E为短周期元素,F为第四周期元素,F还是前四周期中电负极最小的元素。
已知:
A原子的核外电子数与电子层数相等;
B元素原子的核外p电子数比s电子数少1个;
C原子的第一至第四电离能为I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol;
D原子核外所有p轨道为全充满或半充满;
E元素的族序数与周期序数的差为4;
(1)写出E元素在周期表位置:________;D元素的原子的核外电子排布式:____________________。
(2)某同学根据题目信息和掌握的知识分析C的核外电子排布为
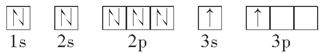
该同学所画的轨道式违背了________。
(3)已知BA5为离子化合物,写出其电子式:______________。
(4)DE3中心原子杂化方式为__________________,其空间构型为______________。
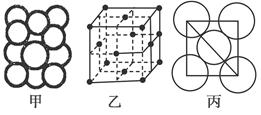
(5)某金属晶体中原子堆积方式如图甲,晶胞特征如图乙,原子相对位置关系如图丙,则晶胞中该原子配位数为________;空间利用率为________;该晶体的密度为________。(已知该金属相对原子质量为m,原子半径为a cm)
参考答案:(1)第三周期ⅦA族 1s22s22p63s23p3
本题解析:(1)由题意分析知F为K;A为H;B为N;由电离能知C的+2价稳定,为Mg;D为P;E为Cl。(2)原子的核外电子分能级排布,按构造原理先排能量低的能级,再排能量高的能级,遵循能量最低原理时,该原子才最稳定。该同学未排满3s能级,就排3p能级,违背了能量最低原理。(3)NH5为离子化合物,则为铵盐,存在NH4+和H-。(4)PCl3中心原子P上的价层电子对=3+
本题难度:一般
2、选择题 美国科学家设想“绿化”火星并使其成为第二个地球:火星上造超级温室气体.美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划.有关全氟丙烷的说法正确的是( )
A.分子中三个碳原子可能处于同一直线上
B.全氟丙烷的电子式为:

C.相同压强下,沸点:C3F8<C3H8
D.全氟丙烷中及既有极性键又有非极性键
参考答案:D
本题解析:
本题难度:简单
3、选择题 元素X、Y、Z原子序数之和为33,X、Y在同一周期,X+与Z2―具有相同的核外电子层结构。下列推测不正确的是(???)??????????
A.同周期元素中X的金属性最强
B.同族元素中Z的氢化物沸点最高
C.原子半径X>Y,离子半径X+> Z2―
D.Y的单质和氧化物有相同的晶体类型
参考答案:C
本题解析:略
本题难度:一般
4、选择题 三氯化氮(NCl3)常温是一种淡黄色液体,其分子结构呈三角锥形,以下关于NCl3的说法中正确的是(???)
A.它是一种非极性分子
B.它能以配位键与Cl-结合,生成NCl4-
C.NCl3中N原子采用SP2杂化
D.已知NCl3中N元素为-3价,所以NCl3水解产物为NH3和HClO
参考答案:D
本题解析:
试题分析:根据分子结构呈三角锥形,可以确定N原子是sp3杂化方式,是极性分子,A、C错。NCl3能提供孤对电子,但是Cl-没有空轨道,所以不能形成配位键,B错。所以正确选项是D。
点评:水解反应属于非氧化还原反应,原分子中显正电的原子或原子团结合水中的OH-,原分子中显负电的原子或原子团结合水中的H+。例如ICl+H2O=HIO+HCl。
本题难度:一般
5、选择题 烃类分子中的碳原子与其他原子的结合方式是[???? ]
A.形成四对共用电子对
B.通过非极性键
C.通过两个共价键
D.通过离子键和共价键
参考答案:A
本题解析:
本题难度:简单