��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ�����������õ��ķ������Խ�����������Fe��Zn��Cu��Pt�Ƚ������ʵĴ����ᴿ������������ȷ���ǣ���֪�����ԣ�Fe2+��Ni2+��Cu2+����������
A������������
B������������ԭ��Ӧ
C���������ӵ�Դ����������缫��ӦΪ��Ni2++2e-�TNi
D�������۵ײ��к���Cu��Pt�Ƚ������ʵ�������
�ο��𰸣�A�������ᴿ�����ݵ��ԭ���ᴿ������������������������������
���������
�����Ѷȣ���
2��ѡ���� �ȼҵ�У��ܴ������ӽ���Ĥ���ǣ�???��
A��Cl��
B��OH��
C��Na��
D��Cl2
�ο��𰸣�C
������������ȼҵ�У����õ��������ӽ���Ĥ����ֻ��Na��ͨ����
�����Ѷȣ���
3��ѡ���� ������ṩ��ͬ�����������£�Cu2+��Ag+�ֱ�Cu2++2e-="Cu" ��Ag++e-=Ag�ڵ缫�Ϸŵ磬������ͭ������Ϊ1.92g����������������Ϊ????????��????��
A��12.96g
B��3.24g
C��6.48g
D��1.62g
�ο��𰸣�C
���������
�������������ͭ�����ʵ�����1.92g��64g/mol��0.03mol��ת�Ƶ��ӵ����ʵ�����0.03mol��2��0.06mol����ؼ������غ��֪�������������ʵ�����0.06mol��������0.06mol��108g/mol��6.48g����ѡC��
�����������Ǹ߿��еij������㣬�ѶȲ�����ȷ�����غ��ǽ���Ĺؼ�������������ѧ���������������淶����������
�����Ѷȣ���
4��ѡ���� �ñ��缫���NaCl��CuSO4��25 0ml�����Һ������һ��ʱ��������ֱ�õ�11.2L����״���£������塣��ԭ��Һ��NaCl�����ʵ���Ũ�Ȳ������ǣ�??��
0ml�����Һ������һ��ʱ��������ֱ�õ�11.2L����״���£������塣��ԭ��Һ��NaCl�����ʵ���Ũ�Ȳ������ǣ�??��
A��0.5mol/L
B��1mol/L
C��1.5mol/L
D��4mol/L
�ο��𰸣�D
�����������
�����Ѷȣ���
5��ѡ���� ����ͼ��a��b��ʯī�缫��ͨ��һ��ʱ���a��������Һ�Ժ�ɫ������˵������ȷ����
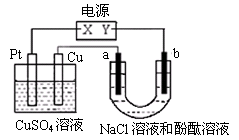
A��X���ǵ�Դ������Y���ǵ�Դ����
B��b���ĵ缫��ӦΪ��2Cl����2e����Cl2��
C����������CuSO4��Һ��Ũ����С
D��Pt������6.4 g Cu����ʱ��a������2.24 L����״��������
�ο��𰸣�C
���������a��������Һ�Ժ�ɫ��˵��a���������������ӷŵ磬�������������ƣ��Լ��ԡ���b����������Һ�е������ӷŵ�����������Y��������X�Ǹ�����Pt����������Һ�е�ͭ���ӷŵ�����ͭ���ʡ�ͭ��������ʧȥ���ӣ�����������ͭ���ӽ�����Һ���ɴ��൱����Pt�ı�����ͭ����Һ�е�����ͭŨ���Dz���ġ����ݵ�ʧ�����غ��֪��6.4gͭת��0.2mol���ӣ������������ʵ�������0.1mol����ѡC��
�����Ѷȣ�һ��