��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ݻ�һ�����ܱ������У���ӦA(g)+2B(g) 2C(g)��ƽ�⣬���ʼA��B�����ʵ����ֱ�ΪXmol��Ymol����Ҫʹƽ��ʱ��Ӧ�������ʵ����������������ʵ�����ȣ���X/YӦ�������
2C(g)��ƽ�⣬���ʼA��B�����ʵ����ֱ�ΪXmol��Ymol����Ҫʹƽ��ʱ��Ӧ�������ʵ����������������ʵ�����ȣ���X/YӦ�������
A��1 <X/Y<3 B��3< X/Y <4
C��0.25< X/Y <1.5 D��0.25< X/Y <0.5
�ο��𰸣�C
���������
�����������μӷ�Ӧ��X�����ʵ���Ϊn��
X��g��+2Y��g�� 2Z��g����
2Z��g����
��ʼ��mol����x y 0
ת����mol����n 2n 2n
ƽ�⣨mol����x-n y-2n 2n
ƽ��ʱ��Ӧ�������ʵ����������������ʵ�����ȣ�������x-n+y-2n=2n�����n=(X+Y)/5��
��Ӧ�ﲻ����ȫ��Ӧ��������x��n��y��2n����x��(X+Y)/5 ��1����y��2(X+Y)/5 ��2��
�⣨1���ã�X/Y��1/4
�⣨2���ã�X/Y��3/2
����1/4��X/Y��3/2����0.25< X/Y <1.5��
��ѡC��
���㣺��ѧƽ����ۺ�Ӧ�� ��ֵ����Ӧ�� ��ѧƽ��ļ���
���������⿼����ǻ�ѧƽ����ۺ�Ӧ��������ֵ����Ӧ�á��Ѷ����ѡ��ؼ��������÷�Ӧ�ﲻ����ȫ��Ӧ���в���ʽ��
�����Ѷȣ�һ��
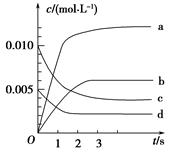
2��ѡ���� ������������ͼ��

���з�Ӧ�з�������ͼ����ǣ� ��
A��2SO3(g) 2SO2(g)��O2(g)����H��0
2SO2(g)��O2(g)����H��0
B��N2(g)��3H2(g) 2NH3(g)����H��0
2NH3(g)����H��0
C��4NH3(g)��5O2(g) 4NO(g)��6H2O(g)����H��0
4NO(g)��6H2O(g)����H��0
D��H2(g)��CO(g) C(s)��H2O(g)����H��0
C(s)��H2O(g)����H��0
�ο��𰸣�A
���������
����������ɵ�һ���͵ڶ���ͼ���֪�����¶��������Ũ������˵��ƽ��������Ӧ�����ƶ���˵������Ӧ���ȣ����ų�B��Cѡ��ɵ�һ�����ڶ����͵��ĸ�ͼ���֪ѹǿ�����������Ũ�ȼ�С��˵��ѹǿ����ƽ�����淴Ӧ�����ƶ�����Ӧ�������ļ�����֮�ʹ�������������Ļ�ѧ������֮�ͣ����ų�Dѡ�
��ѡA��
���㣺����İٷֺ�����Ũ�ȡ�ʱ��ı仯����ѧ��Ӧ�����뻯ѧƽ��ͼ����ۺ�Ӧ��
���������⿼�黯ѧƽ���ƶ�ͼ���⣬��Ŀ�ѶȲ�����Ĺؼ���Ϊ��ȷ����ͼ�������ߵı仯���ƣ����ų��ķ������⡣
�����Ѷȣ�һ��
3������� ��2 L�ܱ������ڣ�800 ��ʱ��Ӧ2NO(g)��O2(g)  2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��(s)
| 0
| 1
| 2
| 3
| 4
| 5
|
n(NO)/mol
| 0.020
| 0.010
| 0.008
| 0.007
| 0.007
| 0.007
?
(1)��ͼ��ʾNO2�ı仯��������________����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��________��
(2)��˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(NO2)��2v(O2)??? b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2)?????? d���������ܶȱ��ֲ���
(3)Ϊʹ�÷�Ӧ�ķ�Ӧ�����������д�ʩ��ȷ����________��
a����ʱ�����NO2����?? b���ʵ������¶�
c������O2��Ũ��???? d��ѡ���Ч����
�ο��𰸣�(1)b��1.5��10��3 mol��(L��s)��1��(2)b
���������(1)NO2����ʼŨ��Ϊc(NO2)��0��2 sʱc(NO2)�ɸ���ͼ����n(NO)�ı仯����⣬c(NO2)��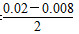 mol��L��1��0.006 mol��L��1���ʴ�ѡb����ͼ������0��2 s��v(NO)�� mol��L��1��0.006 mol��L��1���ʴ�ѡb����ͼ������0��2 s��v(NO)�� �����Ѷȣ�һ�� �����Ѷȣ�һ��
4��ѡ����  ����Ӧ�ﵽƽ��ʱ�����д�ʩ�� ����Ӧ�ﵽƽ��ʱ�����д�ʩ��
�����¢ں���ͨ��������������COŨ�Ȣܼ�ѹ�ݼӴ�����ѹͨ��������壬�����COCl2ת���ʵ��� [???? ]
A���٢ڢ�
B���٢ܢ�
C���ڢۢ�
D���ۢݢ�
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5������� �������������̼���ŵ�һ�ַ����ǣ���ȼú�糧����Ȼ���糧�ŷ����л���CO2������CH4�Ƚ�¯������H2��Ӧ����CH3OH��
CO2��g��+3H2��g�� һ������
CH3OH��g��+H2O��g��
��1��500��ʱ�������Ϊ1L���ݻ��̶����ܱ������У�����1molCO2��3molH2�����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ1��ʾ��
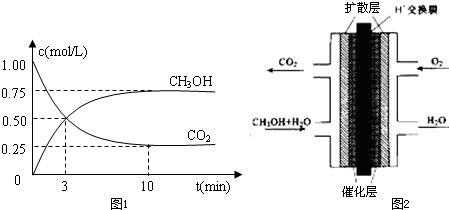
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��=______mol?L-1?min-1��
�ڸ÷�Ӧ��ƽ�ⳣ��K=______������һλС������ƽ��ʱH2��ת����Ϊ______��
����֪�¶����ߣ�Kֵ��С�����д�ʩ����ʹn(CH3OH)
n(CO2)
�������______��
A�������¶�B������He��g����ʹ��ϵѹǿ����
C����H2O��g������ϵ�з���D���ٳ���1molCO2��3molH2
��2��CH3OH��Ϊ��ȼ��ȼ�ϻ�ͨ��ȼ�ϵ�������������ɼ���CO2�ŷŶ��45%��
����֪��
CH3OH��g��+H2O��g���TCO2��g��+3H2��g����H1=+49.0kJ?mol-1
2H2��g��+O2��g���T2H2O��g����H=-483.6kJ?mol-1
��ӦCH3OH��g��+1
2
O2��g���TCO2��g��+2H2��g���ġ�H=______kJ?mol-1��
�ڼ״����ӽ���Ĥȼ�ϵ�صĽṹʾ��ͼ��ͼ2����֪H+����ͨ��O2�ĵ缫���״�����______��������������������������ĵ缫��ӦΪ______��
�ο��𰸣���1������ͼ��֪��10min����ƽ�⣬ƽ��ʱ�״���Ũ�ȱ仯Ϊ
���������
�����Ѷȣ�һ��
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772
|