微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)海水是取之不尽用之不竭的化学资源,从海水中可提取多种化工原料,下图是某化工厂对海水资源综合利用的示意图。
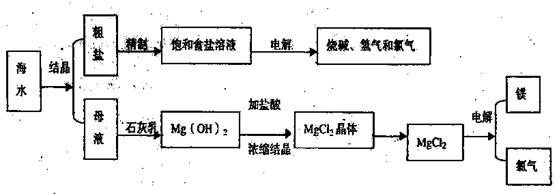
回答下列问题:
(1)请写出电解食盐水的离子方程式????????????????????????。
(2)母液中含有K+、Na+、Mg2+等阳离子,从图中可看出对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是:??????????????。
②石灰乳是生石灰与水作用形成的化合物,从充分利用当地海洋化学资源,提高生产与经济效益的角度考虑,生产生石灰的主要原料是?????????????;
③电解熔融氯化镁的化学方程式是?????????????????????;
④电解无水氯化镁所得的镁蒸气在特定的环境里冷却后可得固态的金属镁,下列物质中可用作镁蒸气的冷却剂是(填写代号)??????????????。
A.H2??????????????????? B.Cl2???????????????????? C.空气?????????????????? D.O2
E.水蒸气
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入一种常见的气态氧化剂,又制取了重要的化工原料溴单质:
①生成溴单质的化学反应的离子方程式是????????????????????????
②以下是对生产溴单质所用的气态氧化剂寻找货源的主凤想,其中合理的是???
(填写代号)
A.以外地购买??????????????????????????????????? B.在当地新建生产厂
C.从本厂生产烧碱外循环?????????????????? D.从木厂生产镁单质处循环
③从各种经营综合开发,打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目是??????。
参考答案:
(1)2Cl-+2H2O 本题解析:略
本题解析:略
本题难度:简单
2、填空题 过氧化钙(CaO2)难溶于水,在常温下稳定,在潮湿空气及水中缓慢分解放出氧气,因而广泛应用于渔业、农业、环保等许多方面。下图是以大理石(主要杂质是氧化铁)等为原料制取过氧化钙(CaO2)的流程。
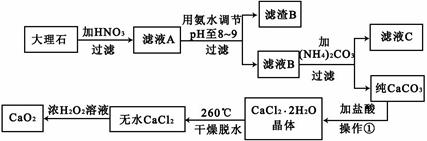
请回答下列问题:
(1)用氨水调节pH至8――9的目的是???????????????。
(2)若测得滤液C中c(CO32-)=10-3mol/L,则Ca2+???????(填“是”或“否”)沉淀完全。(已知c(Ca2+)≤10-5mol/L可视为沉淀完全;Ksp(CaCO3)=4.96×10-9)
(3)若在滤液C中,加入HNO3使溶液呈酸性以得到副产物NH4NO3,则酸化后溶液中,c(NH4+) ????c(NO3-)(填“≥”、“≤”、“<”、“>”或“=”)。
(4)在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,写出该反应的化学方程式:????????????????????????????,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至9――11,才出现大量沉淀。用化学方程式和简要的文字解释需用氢氧化钠调节pH至9――11的原因??????????????????????????????????????????????。
参考答案:(1)除去Fe3+?; (2)是?;(3)<;
(4)
本题解析:
试题分析:根据图示信息,可得出:滤液A的成分有硝酸钙和硝酸铁以及剩余的硝酸,当pH至8-9范围段内时,三价铁可易形成沉淀,所以滤渣B是氢氧化铁,滤液B是硝酸钙,和碳酸铵之间可以发生复分解反应生成碳酸钙和硝酸铵,过滤,沉淀碳酸钙用盐酸溶解然后蒸发结晶可以得到氯化钙晶体,再失水成为无水氯化钙,双氧水可以和氯化钙反应生成过氧化钙和盐酸.
(1)用氨水调节pH至8-9,三价铁可易形成沉淀,从而分离出硝酸钙溶液,故答案为:除去Fe3+;
(2)若测得滤液C中c(CO32-)=10-3 mol/L
本题难度:困难
3、选择题 水资源非常重要,虽然地球70%的面积被海水所包围,但淡水的比例只有2.5%,且其中绝大部分以冰川和其他形式存在,实际能够用来饮用的水不足全球淡水总量的1%。下列关于水的说法错误的是( )。
A.蒸馏法是海水淡化的方法之一
B.淡水的密度小于海水的密度
C.融化的雪水中矿物质含量比深井水中的少
D.0 ℃以上,温度越高,水的密度越小
参考答案:D
本题解析:海水中含有Na+、Mg2+、Cl-及SO42―等,这些离子所组成的物质的沸点比水的沸点高,可用蒸馏的方法将其分离,A项正确;上述杂质的溶入使海水的密度大于淡水,B项正确;雪与雨水成分相同,是水蒸发后凝结而成的,含矿物质很少,而深井中的水不断与硅酸盐矿物质接触,其中溶有许多矿物质,C项正确;由于水在4 ℃时密度最大,因此在0~4 ℃之间,温度越高水的密度越大,而在4 ℃以上时,温度越高水的密度越小,D项错误。
本题难度:简单
4、选择题 粗碘中通常含ICl和IBr,称为卤素互化物,其性质和卤素单质相似,都是较强的氧化剂,而且受热时ICl和IBr皆可像I2一样升华,在粗碘中加入以下选项中的一种物质后,再进行升华可制得精碘,应加入的物质是( )。
A.H2O
B.Zn
C.KI
D.KCl
参考答案:C
本题解析:利用碘升华的特性精制碘,须使ICl、IBr中的Cl、Br变为难挥发性的物质,同时使其中+1价的碘被还原为单质碘,且加入的物质和碘不反应,只有KI符合,化学方程式为ICl+KI=I2+KCl,IBr+KI=I2+KBr。
本题难度:一般
5、选择题 下列冶炼方法中,可将化合物中的金属元素还原为金属单质的是
A.加热Al2O3
B.加热CaCO3
C.电解熔融NaCl
D.氯化钠与铝粉高温共热
参考答案:C
本题解析:
试题分析:A、铝是活泼的金属,只能通过电解法冶炼,因此电解熔融的氧化铝可以获得金属铝,A不正确;B、钙是活泼的金属,只能通过电解法冶炼。加热碳酸钙分解生成氧化钙和CO2,B不正确;C、钠是活泼的金属,只能通过电解法冶炼,因此电解熔融的氯化钠可以得到钠,C正确;D、钠是活泼的金属,且活泼性强于铝,金属铝与氯化钠不可能发生铝热反应,D不正确,答案选C。
本题难度:一般