微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如下图:
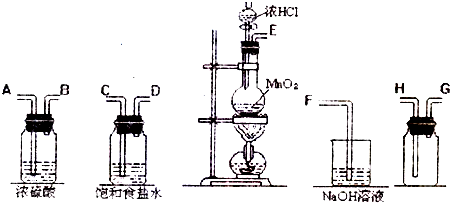
(1)连接上述仪器的正确顺序是(填各接口处的字母):E接______,______接______,______接H,G接F.
(2)在装置中;①饱和食盐水起的作用是______;②浓硫酸起的作用是______.
(3)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸.如果有Cl2产生,可观察到的现象是______,写出反应方程式______.
(4)写出下列化学反应的离子方程式
①气体发生装置中进行的反应:______;
②尾气吸收装置中进行的反应:______.
2、实验题 (1)写出实验室制氨气的化学方程式:_____________________________________________。
(2)在下图方框内画出氨气的收集装置(夹持装置可略去)
3、选择题 实验室制氯气时有如下操作,操作顺序排列正确的是[???? ]
①连接好装置,检查装置的气密性②缓缓加热③在烧瓶中加入少量的MnO2,分液漏斗中加入浓盐酸④从分液漏斗中慢慢向烧瓶中注入浓盐酸⑤将多余氯气用NaOH溶液吸收⑥用向上排气法收集氯气
A.①②③④⑤⑥
B.③④②①⑥⑤
C.①④③②⑥⑤
D.①③④②⑥⑤
4、简答题 某校化学兴趣小组的同学利用漂白粉与稀硫酸在加热条件下反应制取Cl2,其反应的化学方程式为:Ca(ClO)2+CaCl2+2H2SO4
??△??
.
?
2CaSO4+2Cl2↑+2H2O.以下是制取Cl2并验证其部分性质的实验装置.

试回答下列问题:
(1)请在上图(右上装置中)选择满足实线框图I的气体发生装置:______(填代号);
(2)实验装置Ⅲ的作用是______;
(3)一段时间后,装置Ⅲ的溶液仍呈强碱性,其中肯定存在Cl-、OH-和SO42-,请设计实验探究该吸收液中可能存在的其它阴离子(不考虑空气中CO2的影响).
①提出合理假设:假设1:只存在SO32-;???假设2:只存在ClO-;???假设3:______
②设计实验方案进行实验,请写出实验步骤以及预期现象和结论.实验试剂:3mol?L-1?H2SO4、1mol?L-1?NaOH、0.01mol?L-1?KMnO4、淀粉KI溶液、紫色石蕊试液. | 实验步骤 | 预期现象和结论
步骤1:取少量吸收液于试管中,滴加3mol?L-1 H2SO4至溶液显酸性,然后将所得溶液分置于A、B试管中.
/
步骤2:______
______?
步骤3:______
______?
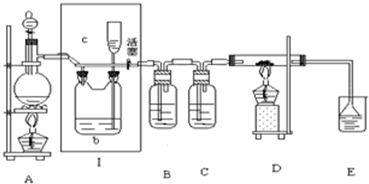
5、填空题 如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为:B(碘化钾淀粉溶液),C(水),E(紫色石蕊试液).
(1)A是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,分液漏斗中盛放浓盐酸,实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃D处酒精灯.请回答以下问题:
①怎样证明氯气已经充满了整个装置______;
②B中的实验现象是______.
(2)在D装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,一种产物能使E处紫色石蕊试液变红,另一产物能使澄清石灰水变浑浊,根据信息写出D中反应的化学方程式______.
(3)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是______.
(4)D处反应完毕后关闭分液漏斗旋塞,移去酒精灯,但由于余热的作用,A处仍有氯气产生,此时应该怎样操作______;装置Ⅰ中的现象是______.
(5)若将C中的水换成氢氧化钠溶液,溶液中不但有NaClO还有NaClO3,其物质的量比为2:1,则参加反应的氧化剂和还原剂的物质的量比为:______.
|
|
网站客服QQ: 960335752 - 14613519 - 791315772