微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO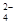 ?等离子,电极为惰性电极。下列叙述中正确的是
?等离子,电极为惰性电极。下列叙述中正确的是

A.A膜是阳离子交换膜
B.通电后,海水中阴离子往b电极处运动
C.通电后,b电极上产生无色气体,溶液中出现白色沉淀
D.通电后,a电极的电极反应式为:4OH--4e- = O2↑+2H2O
参考答案:C
本题解析:
试题分析:A.A膜是阴离子交换膜。错误。B.通电后,海水中阴离子往正电荷较多的阳极a电极处运动.错误。C.通电后,由于放电能力H+>Mg2+>Ca2+,所以H+在阴极b电极上放电:2H++2e-=H2↑.产生无色气体,由于破坏了附近的水的电离平衡,在该区域c(OH-)增大,会发生反应:Mg2++2OH-=Mg(OH)2↓所以溶液中还出现白色沉淀。正确。D.通电后,由于在溶液中的放电能力Cl->SO 本题难度:一般
本题难度:一般
2、选择题 在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,最好选用[???? ]
A.NaOH
B.HCl
C.NaCl
D.CuSO4
参考答案:A
本题解析:
本题难度:一般
3、填空题 (17分)铜在工农业生产中有着广泛的用途。
(1)配制CuSO4溶液时需加入少量稀H2SO4,其原因是 (只写离子方程式)。
(2)某同学利用制得的CuSO4溶液,进行以下实验探究。
①图甲是根据反应Fe+CuSO4=Cu+FeSO4设计成铁铜原电池,请图甲中的横线上完成标注。
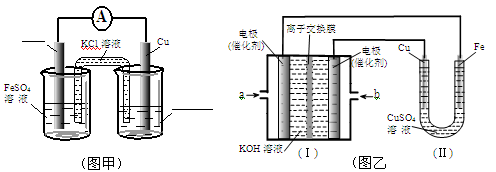
②图乙中,I是甲烷燃料电池的示意图,该同学想在II中实现铁上镀铜,则应在a处通入 (填“CH4”或“O2”),b处电极上发生的电极反应式为 ==4OH-;
若把II中电极均换为惰性电极,电解液换为含有0.1molNaCl溶液400mL,当阳极产生的气体为448mL(标准状况下)时,溶液的pH= (假设溶液体积变化忽略不计)。
(3)电池生产工业废水中常含有毒的Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去[室温下Ksp(FeS)=6.3×10-18mol2・L-2,Ksp(CuS)=1.3×10-36mol2・L-2]。请结合离子方程式说明上述除杂的原理:当把FeS加入工业废水中后,直至FeS全部转化为CuS沉淀,从而除去溶液中Cu2+。
参考答案:(1)Cu2++2H2O 本题解析:
本题解析:
试题分析:(1)加入稀硫酸是为了抑制Cu2+的水解;(2)图乙在Fe上镀铜,所以Fe作阴极,则连接的为燃料电池的负极,应通入CH4,b极通入O2发生还原反应:O2+4e-+2H2O =4OH-;电解池中均为惰性电极时,阳极的电极反应式为:2Cl--2e-=Cl2↑ ,阴极反应式为:2H++2e-=H2 ↑ .由电极反应式计算消耗的H+为0.04mol,则生成的OH-为0.04mol,c(OH-)=0.1mol/L,则c(H+)=10-13mol/L,pH=13;(3)应用了难溶电解质的沉淀溶解平衡,溶液中存在溶解平衡:FeS(s)  Fe 2+(aq)+ S 2-(aq),Cu2+与S 2-反应可生成溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动。
Fe 2+(aq)+ S 2-(aq),Cu2+与S 2-反应可生成溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动。
考点:盐类水解、原电池原理及计算、难溶电解质的沉淀溶解平衡。
本题难度:困难
4、选择题 在盛有饱和碳酸钠溶液的烧杯里,插入惰性电极,接通直流电源,保持温度不变,一定时间后,溶液中
A.Na2CO3浓度减少
B.Na2CO3浓度增大
C.Na2CO3浓度增大,并有晶体析出
D.Na2CO3浓度不变,并有晶体析出
参考答案:D
本题解析:略
本题难度:简单
5、选择题 右图装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中所列各项对应关系均正确的一组是:

选项
| 电源X极
| 实验前U形????管中液体
| ?通电后现象及结论
|
A
| 正极
| Na2SO4溶液
| U形管两端滴入酚酞后,a管中呈红色
|
B
| 正极
| AgNO3溶液
| b管中电极反应式是?? 4OH― -4e-=2H2O+O2↑
|
C
| 负极
| KCl和CuCl2混合溶液
| 相同条件下,a、b两管中产生的气体总体积可能相等
|
D
| 负极
| Fe(OH)3胶体和导电液
| b管中液体颜色加深
?
参考答案:
C
本题解析:
本题考查电化学知识;电解硫酸钠溶液的实质是电解水,H+在阴极区放电,OH-在阳极区放电,促进了水的电离,故在阴极区有大量的OH-,滴入酚酞后,b管中呈红色,A项错误;电解硝酸银,Ag+在阴极放电,电极反应式为: 4Ag+ +4e- ==4Ag,OH-在阳极反应:4OH- +4e- ==2H2O+O2↑,B项错误;氢氧化铁胶体带正电荷,在A管中液体颜色加深,D项错误。
本题难度:一般
|