微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 有一瓶溶液只含Cl-、CO32-、SO42-、Na+、K+、Mg2+六种离子中的某几种.经实验:
①原溶液
过量NaOH
白色沉淀;
②原溶液中加BaCl2溶液不产生沉淀;
③原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解
回答下列问题:
(1)试分析原溶液中一定含有的离子是______,一定不含有的离子是______,可能含有的离子是______
(2)有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)______说明理由______.
参考答案:(1)溶液中加入过量NaOH生成白色沉淀,说明溶液中含有Mg
本题解析:
本题难度:一般
2、选择题 NA表示阿伏加德罗常数的值,下列说法中正确的是
A.常温常压下,0.05 NA个CO2分子所占的体积是1.12L
B.氨气的摩尔质量和NA个氨分子的质量相等
C.常温常压下,32g O2和34g H2S气体分子个数比为1:1
D.标准状况下, NA个水分子所占的体积约为22.4L
参考答案:C
本题解析:
试题分析:A项的温度和压强应该是标准状况下,B项氨气的摩尔质量在数值上和NA个氨分子的质量相等,摩尔质量是个物理量不能和质量相等,D项水标准状况下是固态,不能用22.4L来表示。答案选C。
点评:阿伏伽德罗常数是历年高考的“热点”问题。多年来全国高考化学试题出现的几率为100%。这双因为它既考查了学生对物质的量与粒子数、质量、气体体积和物质的量浓度之间的关系,又可以与物质结构、盐类水解、弱电解质的电离等其他的概念性知识点结合成综合性习题。
本题难度:一般
3、选择题 设阿伏伽德罗常数的值为NA,标准状况下某种O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积应是
A.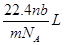
B.
C.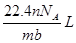
D.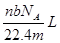
参考答案:A
本题解析:
试题分析:设阿伏伽德罗常数的值为NA,标准状况下某种O2和N2的混合气体mg含有b个分子。
解:mg气体有b个分子,
ng气体就有(b×n/m)个分子,
这些分子的物质的量就是[(b×n/m)/NA]mol,
这些气体所占的体积V=[(b×n/m)/NA]×22.4,
化简一下就是:V=22.4nb/(mNA).
故选A。
点评:气体摩尔体积使用时应注意:
①必须是标准状况。②“任何理想气体”既包括纯净物又包括气体混合物。
③气体摩尔体积通常用
本题难度:一般
4、实验题 (6分) 11.欲用18 mol/L的浓硫酸(密度为1.84g/mL)配制成浓度为 0.5mol/L 的稀硫酸 500mL。
(1)选用的主要仪器有:烧杯、量筒、胶头滴管、玻璃棒和_________ 。
(2)请将下列各操作按正确的序号填写在横线上__________。
A.用量筒量取浓硫酸
B.反复颠倒摇匀
C.用胶头滴管加水至刻度
D.将配制好的溶液转入试剂瓶中贴上标签
E.稀释浓硫酸 F.将溶液转入容量瓶
(3)简要回答下列问题:
①所需浓硫酸的体积为______mL;
②如果实验室有15mL 、20mL、50mL的量筒,应选用_____mL。
参考答案:(1)500ml容量瓶????(2) AEFCBD????(
本题解析:(1)根据配制过程可知,还需要500ml容量瓶。
(2)根据配制原理可知,正确的顺序是AEFCBD。
(3)①溶质的物质的量是0.5L×0.5mol/L=0.25mol,所以需要浓硫酸的体积0.25mol÷18mol/L=0.0136L=13.6ml。
②根据规格相近的原则可知,应该选择15ml量筒。
本题难度:一般
5、选择题 在a?L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b?mol的BaCl2,恰好使溶液中的SO42-完全沉淀;如加入足量强碱并加热可得到c?mol NH3,则原溶液中的Al3+的浓度(mol?L-1)为( )
A.
b-2c
2a
B.2b-c
a
C.2b-c
3a
D.c-2b
6a
参考答案:由混合溶液中加入bmolBaCl2,恰好使溶液中的SO42-
本题解析:
本题难度:一般
|
|
|
网站客服QQ: 960335752 - 14613519 - 791315772
|