微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于化学反应说法中正确的是
A.化学键的断裂和形成是化学反应中能量变化的主要原因
B.化学反应速率为0.8 mol /(L・s)是指1s 内生成0.8mol该物质
C.可逆反应达到平衡时,各物质的质量不变,
D.化学反应的限度不可以通过改变条件而改变
2、选择题 已知:4NH3+5O2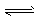 4NO+6H2O,若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O) [mol・L-1・min-1]表示,则下列关系正确的是?
4NO+6H2O,若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O) [mol・L-1・min-1]表示,则下列关系正确的是?
[???? ]
A. υ(NH3)=υ(O2)=υ(NO)=υ(H2O)
B. υ(NH3):υ(O2):υ(NO):υ(H2O)= 4:5:4:6
C. υ(NH2)= 3/2υ(H2O)
D. 5υ(O2)=6υ(H2O)
3、选择题 在一定条件下,某密闭容器内,SO2氧化成SO3的热化学方程式为:2SO2(g)+O2(g) 2SO3(g);△H =-a kJ・mol-1。在相同条件下,要想得到2a kJ的热量,加入各物质的物质的量可能是????????????????????????????????????????[???? ]
2SO3(g);△H =-a kJ・mol-1。在相同条件下,要想得到2a kJ的热量,加入各物质的物质的量可能是????????????????????????????????????????[???? ]
A.4mol SO2和2mol O2
B.5mol SO2和3mol O2
C.4mol SO2和4mol O2
D.4mol SO2、2mol O2和2mol SO3
4、选择题 相同温度下,体积均为0.5?L的两个恒容密闭容器中发生可逆反应:
2XY2(g) + Y2(g)  ?2XY3(g)???△H=-Q kJ・mol-1(Q>0)
?2XY3(g)???△H=-Q kJ・mol-1(Q>0)
实验测得反应在起始、达到平衡时的有关数据如下表所示:
容器
编号
| 起始时各物质物质的量/mol
| 达平衡时体系能量的变化
|
XY2
| Y2
| XY3
|
①
| 2
| 1
| 0
| 放热 0.25 Q kJ
|
②
| 1.2
| 0.6
| 0.8
| ?
下列叙述不正确的是
A.容器①、②中反应的平衡常数均为1/13.5
B.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol・L-1
C.容器②中反应达到平衡时放出的热量为0.15 Q kJ
D.若容器①的其他条件不变,恒压下通入稀有气体,则达到平衡时放出的热量小于0.25 Q kJ
5、选择题 对于可逆反应N2+3H2 2NH3下列各项所表示的反应速率最快的是???? [???? ] 2NH3下列各项所表示的反应速率最快的是???? [???? ]
A.??V(N2)=0.01mol/(L・s)??????????????
B.??V(H2)=0.2mol/(L・s)
C.??V(H2)=0.6mol/(L・s)?????????????
D.??V(NH3)=1.2mol/(L・s)
|