��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ���¶��£���a L�ܱ������м���һ����A��B���壬�������·�Ӧ��A2(g)+3B(g)  2C2 (g)+2D(g)��������Ϊ��Ӧ�ﵽƽ��ı�־��(C??? )
2C2 (g)+2D(g)��������Ϊ��Ӧ�ﵽƽ��ı�־��(C??? )
A����������ѹǿ����ʱ��仯���仯
B����λʱ���ڶ���һ��A-A����ͬʱ��������C-C��
C��v��(B)=0.03mol/(L?s)��v��(D)=1.2mol/(L?min)
D�������������ƽ����Է�����������ʱ��仯���仯
�ο��𰸣�C
�����������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬����Ӧǰ��������䣬����ѹǿʼ���Dz���ģ�A����ȷ��B�з�Ӧ���ʵķ�������ͬ�ģ�����ȷ��C�з�Ӧ���ʵķ����෴������������֮������Ӧ�Ļ�ѧ������֮�ȣ���ȷ���������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ�����������ʵ������Dz���ģ�����D����ȷ����ѡC��
�����Ѷȣ���
2��ѡ���� Ϊ�˼��������������ڲ�ͬ�¶��¶Ա��������Ӱ�졣����������ͬ����ʱȡ�������ɷ֣�
�¶�/��
| 85
| 90
| 95
| 100
| 200
| 280
| 300
| 320
| 340
|
��(mmol)
| 96.05
| 91.30
| 91.55
| 80.85
| 10
| 23.35
| 36.90
| 55.99
| 72.37
|
������
(mmol)
| 3.95
| 8.7
| 8.45
| 19.15
| 90
| 76.65
| 63.10
| 44.01
| 27.63
(�����ͷ�Ӧװ�ã�ѹǿΪ0.78 MPa���⡢�����ʵ���֮��Ϊ6.5��1)
����˵���������
A�����ŷ�Ӧ�¶ȵ����ߣ�����ת���������ߺ�
B��ͨ���ı��¶Ȼ�ѹǿ����ʹ�����ͱ���ת������ͬ
C������ѹǿ���⡢�����ʵ���֮�ȿ�����������߱���ת����
D�����¶ȳ���280 �棬����ת����Ѹ���½�����������Ϊ�÷�ӦΪ���ȵĿ��淴Ӧ
�ο��𰸣�D
������������ݱ������ݵı仯���ƿ���AC��ȷ���¶Ȼ�ѹǿ��Ӱ�컯ѧƽ�⣬B��ȷ��������Ӧ���ȣ����¶��������������ת���ʣ����÷�ӦӦ�Ƿ��ȷ�Ӧ��D����ȷ��
�����Ѷȣ�һ��
3��ѡ���� ��ӦI2+I- I3-�ﵽƽ��ʱc(I3-)���¶ȵĹ�ϵ��ͼ��ʾ�� I3-�ﵽƽ��ʱc(I3-)���¶ȵĹ�ϵ��ͼ��ʾ��
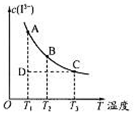
����˵����ȷ����
A��ͼ�з�Ӧ���е�״̬Dʱ��һ����v��>v��
B��A���B��Ļ�ѧƽ�ⳣ����ͬ
C����B����Һ�����¶�ʱ���÷�Ӧ��v��>��v��
D������KI��ҺŨ��������I2���ܽ�
�ο��𰸣�D
���������
���������A��B��C���㶼�Ǵ���ƽ�������ϣ�����ƽ��״̬��A ��ͼ�з�Ӧ���е�״̬Dʱ����ʱ��Ӧ���¶���T1��A�����ƽ��״̬��D�Dz�ƽ��״̬����D��A��������ƽ������У�c(I3-)����˵����ӦҪ���ֽ��У�����һ����v��>v�档A����B��A���B��Ļ�ѧƽ�ⳣ������ͬ����ΪT1�� T2������ͬ�¶ȡ�C����A��C�����У��¶������ߣ�c(I3-)��С��ƽ�������ƶ���˵���淴Ӧ���ȣ�����Ӧ���ȡ����Զ�B����Һ�����¶�ʱ��ƽ�����淴Ӧ�����ƶ����÷�Ӧ��v��>��v����D������KI��ҺŨ�ȣ�ƽ��������Ӧ�����ƶ�����Ȼ������I2���ܽ�
�����Ѷȣ�һ��
4�������� ��Ҫ��������и�С�⡣???
��CO��H2�Ļ�������׳ƺϳ�������һ����Ҫ�Ĺ�ҵԭ��������̿����Ȼ������Ҫ�ɷ�ΪCH4�������͡�ú�ڸ����¾�����ˮ������Ӧ�Ƶúϳ�����
��1����֪ij��Ӧ��ƽ�ⳣ������ʽΪ��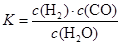 ? ?
������Ӧ�Ļ�ѧ����ʽΪ��????????????????????????????????????????????????��
��2�������Ϊ2L���ܱ������г���CH4��H2O(g)��ɵĻ��������1mol������һ�������·�����Ӧ�����ﵽƽ��״̬������¶ȡ�ѹǿ��Ͷ�ϱ�X��n(CH4)/n(H2O)���Ը÷�Ӧ��Ӱ����ͼ��ʾ��
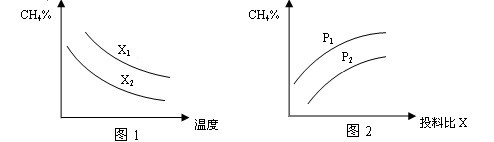
��ͼ1�е�����������ʾͶ�ϱȵĹ�ϵX2 ____ X1(�=����>����<����ͬ)
��ͼ2������������ʾ��ѹǿ�ȵĹ�ϵ��P2 _______P1
��3����CH4��O2Ϊԭ�Ͽ���Ƴ�ȼ�ϵ�أ�
����װ����ʢ��150.0mL 1.0mol/L KOH��Һ���ŵ�ʱ���뷴Ӧ�������ڱ�״���µ����Ϊ4.48L������ŵ������û�������ݳ�����ŵ���Ϻ�������Һ�и�����Ũ���ɴ�С�Ĺ�ϵΪ��?????????
����H2SO4��Һ����KOH��ҺΪ�������Һ,��CH4��ΪC6H12O6 ����ȼ�ϵ�صĸ�����ӦʽΪ��
????????????????��
��1��ij�¶�(t��)ʱ�����0.01mol��L-1��NaOH��Һ��pH��11���ڴ��¶��£���pH��2��H2SO4��ҺVaL��pH��12��NaOH��ҺVbL��ϣ������û��ҺΪ���ԣ���Va�UVb��??????????��
(2)��25��ʱ����c mol��L-1�Ĵ�����Һ��0.02 mol��L-1NaOH��Һ�������Ϻ���Һ�պó����ԣ��ú�c�Ĵ���ʽ��ʾCH3COOH�ĵ��볣��Ka=____________________��
�ο��𰸣���14�֚���2�֣�
��1�� C��S��+H2O(g)
���������
�����������1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը���ƽ�ⳣ���ı���ʽ��֪���÷�Ӧ�Ļ�ѧ����ʽ��C��S����H2O(g) H2(g)��CO(g)�� H2(g)��CO(g)��
��2���ٸ��ݷ�Ӧ�Ļ�ѧ����ʽCH4��H2O CO��3H2��֪�����¶���ͬʱ��Ͷ�ϱ�Խ�����ת����Խ�ͣ��������м���ĺ���Խ�ߣ����Ը���ͼ��1��֪��X2��X1�� CO��3H2��֪�����¶���ͬʱ��Ͷ�ϱ�Խ�����ת����Խ�ͣ��������м���ĺ���Խ�ߣ����Ը���ͼ��1��֪��X2��X1��
�ڸ��ݷ���ʽ��֪���÷�Ӧ���������ģ�������Ͷ�ϱ���ͬ�������£�ѹǿԽ�����ת����ԽС�������ĺ���Խ�ߣ����Ը���ͼ 2��֪��P2��P1��
��3�����ڸ�ȼ�ϵ���У������ڸ���ͨ�룬����������ͨ�롣�μӷ�Ӧ��������0.2mol���õ�0.8mol���ӣ��������ļ�������ʵ�����0.8mol��8��0.1mol������CO2��0.1mol������Һ������������0.15mol�����Է�Ӧ������̼��غ�̼����أ��Ҷ��ߵ����ʵ�������0.05mol������CO32����ˮ��̶ȴ���HCO3����ˮ��̶ȣ����Էŵ��������Һ�и�����Ũ���ɴ�С�Ĺ�ϵΪc(K+)��c(HCO3-)��cCO32-)��c(OH-)��c(H+)��
��ԭ����и���ʧȥ���ӣ������������ڸ����ŵ磬�缫��Ӧʽ��C6H12O6��24e-+6H2O��6CO2��24H+��
��1��ij�¶�(t��)ʱ�����0.01mol��L-1��NaOH��Һ��pH��11�����Ը��¶���ˮ�����ӻ�������1��10��13������pH��12��NaOH��Һ��OH����Ũ����0.1mol/L�����û��ҺΪ���ԣ���˵������ǡ�÷�Ӧ����VaL��0.01mol/L��VbL��0.1mol/L�����Va�UVb��10�U1��
��2����25��ʱ����c mol��L-1�Ĵ�����Һ��0.02 mol��L-1NaOH��Һ�������Ϻ���Һ�պó����ԣ���˸��ݵ���غ��֪����Һ��c(CH3COO��)��c(Na��)��0.01mol/L������Һ��c(CH3COOH)����0.5c��0.01��mol/L������Ϊ��Һ��c(H��)��1��10��7mol/L�����Ը��ݴ���ĵ��볣������ʽ��֪Ka��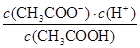 ��2��10-9/��c��0.02���� ��2��10-9/��c��0.02����
�����Ѷȣ�����
5������� һ���¶�����10L�����м���5molSO2��3molO2������Ӧ�ﵽƽ��ʱ����3molSO2�����˷�Ӧ����
��1��������_________molSO3��SO2��ת����Ϊ_________���ðٷ�����ʾ����
��2��ƽ��ʱ����������������ʵ���Ϊ_________��
��3��ƽ��ʱSO2��Ũ����_________ ��O2��Ũ����_________��SO3��Ũ����_________ ��
�ο��𰸣�
 ����������� �����������
�����Ѷȣ�һ��
|