微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)按下列要求各举一例,写出有关化学方程式,并标出电子转移的方向和数目。
(1)氢气还原一种非金属单质______________________
(2)同一种物质中的一种元素被氧化,另一种元素被还原________________
(3)同种元素不同物质间的氧化还原反应__________________________
(4)一种固体非金属单质置换另一种气体非金属单质______________________
参考答案:27、每空2分,共8分。其它符合题意亦可。
(1)
本题解析:
试题分析:(1)氢气还原一种非金属单质,常见反应是H2燃烧,如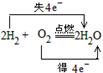
(2)同一种物质中,一种元素氧化另一种元素,反应物只有一种,生成物中有单质生成的分解反应,如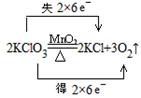
(3)同种元素不同物质间的氧化还原反应,常见的是归中反应,如: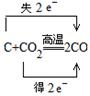
(4)一种固体非金属单质置换另一种气体非金属单质,该反应为置换反应,如
考点:考查氧化还原反应电子转移的表示方法。
本题难度:一般
2、填空题 (8分)一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。
⑴在人体中进行的 转化时,②中的Fe3+作 剂;
转化时,②中的Fe3+作 剂;
⑵ “服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作 剂,具有 性。
⑶市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为 。
参考答案:(1)氧化(2)还原,还原(3)Fe+2H+=H2↑+Fe2
本题解析:(1)Fe3+转化为Fe2+,化合价降低,作氧化剂。
(2)铁离子具有氧化性,作氧化剂,所以维生素C是还原剂,具有还原性。
(3)胃酸显酸性,和铁生成生成亚铁离子和氢气。
本题难度:一般
3、填空题 已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。在含3 molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,试回答下列问题:
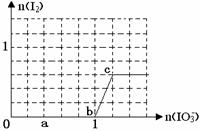
(1)写出a点反应的离子方程式 ;
反应中还原剂是 ;被还原的元素是 。
(2)写出b点到c点反应的离子方程式 。
(3) 当溶液中的I-为0.4 mol时,加入的KIO3为 mol。
当溶液中的I-为0.4 mol时,加入的KIO3为 mol。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为
。
参考答案:(1)IO3-+ 3HSO3-→I-+ 3SO42-+3H+
本题解析:略
本题难度:一般
4、选择题 下列各变化中属于原电池反应的是
A.在空气中金属铝表面迅速氧化形成保护层
B.镀锌铁皮表面有划损时,仍然能阻止铁被氧化
C.红热的铁丝与水接触,表面形成蓝黑色保护层
D.纯锌与稀硫酸反应时,有大量气泡产生
参考答案:B
本题解析:属于原电池反应要符合原电池的形成条件;活性不同的两电极,电解质溶液,闭合电路。故B符合。Zn-Fe原电池,Zn为负极,保护Fe。
本题难度:一般
5、填空题 镁与稀硝酸的反应为:Mg+ HNO3(稀)―― Mg(NO3)2+ NH4NO3+ H2O
(1)配平上述化学方程式并用“双线桥法”表示该反应中电子转移的方向和数目。
(2)该反应中,还原产物是_________,HNO3表现了________(选填“还原性”、“氧化性”、“酸性”、“碱性”)。
(3)若反应过程中转移的电子数为6.02×1023,则被还原的硝酸物质的量为________。
参考答案:
(1) 本题解析:
本题解析:
试题分析:(1)Mg+ HNO3(稀)―― Mg(NO3)2+ NH4NO3+ H2O,Mg由0价变成了+2价化合价↑2,N由+5价变成了-3价↓8,最小公倍数是8,Mg系数×4,Mg(NO3)2系数×4,通过观察反应前后N守恒,HNO3系数×10,最后H守恒,H2O×3,得出:4Mg+10HNO3(稀)="==" 4 Mg(NO3)2+NH4NO3+3H2O;(2)N的化合价降低被还原,同时反应后NO3-的存在,因此NH4NO3是还原产物,HNO3既表现氧化性,又表现酸性;(3)HNO3→NH4NO3,生成1molNH4NO3时,共转移8mole-,现在转移了6.02×1023个电子,则被还原的硝酸的物质的量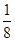 mol=0.125mol。
mol=0.125mol。
考点:考查氧化还原反应电子转移的表示方法、化学方程式的配平及计算。
本题难度:一般