��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��7�֣����о�֪Cu2����H2O2�ֽ�Ҳ���д����ã�Ϊ�Ƚ�Fe3����Cu2����H2O2�ֽ�Ĵ�Ч����ij�о�С���ͬѧ�ֱ��������ͼ�ס�����ʾ��ʵ�顣�ش�������⣺
(1) ���Է�������ͼ��ͨ���۲�________________________________�����ԱȽϵó����ۡ���ͬѧ�����FeCl3��ΪFe2(SO4)3��Ϊ��������������__________________________________��д��H2O2��MnO2�����·�����Ӧ�Ļ�ѧ����ʽ��______________________________��

(2) ������������ͼ����ʾ��ʵ��ʱ��������40 mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԡ�ͼ������A������Ϊ__________��ʵ������Ҫ������������_???? _______________��
2������� ��ҵ��һ���ں����ܱ������п��Բ������з�Ӧ�ϳɼ״���CO��g��+2H2��g��?CH3OH��g��
��1���жϷ�Ӧ�ﵽƽ��״̬�������ǣ�����ĸ��ţ���ͬ��______��
A������CH3OH������������CO���������
B�����������ܶȲ���
C�������������ƽ��������������
D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
��2��������������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 250�� | 300�� | 350��
K
2.041
0.270
0.012
���ɱ��������жϸ÷�Ӧ�ġ�H______0�����������=����������
��ij�¶��£���2molCO��6molH2����2L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c��CO��=0.2mol/L����CO��ת����Ϊ______����ʱ���¶�Ϊ______��
��3��Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��______��
a������b���������c������CO��Ũ��
d������H2��ѹe��������������ѹf��������״�
��4��һ�������£�CO��H2�ڴ���������������5molCH3OH�������仯Ϊ454kJ���ڸ��¶�ʱ�����ݻ���ͬ��3���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
| ���� | �� | �� | ��
| ��Ӧ��Ͷ����
1molCO��2molH2
1molCH3OH
2molCH3OH
| ƽ��ʱ����
CH3OH��Ũ�ȣ�mol/L��
c1
c2
c3
��Ӧ�������仯
akJ
bkJ
ckJ
��ϵѹǿ��Pa��
p1
p2
p3
��Ӧ��ת����
��1
��2
��3
����˵����ȷ����______��
A.2c1��c3B��a+b��90.8C.2p2��p3D����1+��3��1��
3������� �״�����Ϊ21���͵�����ȼ�ϣ���ҵ��ͨ�����з�Ӧ��͢���CH4��H2OΪԭ�����Ʊ��״���
(1)��1.0 mol CH4��2.0 mol H2O(g)ͨ�뷴Ӧ��(�ݻ�Ϊ100 L)����һ�������·�����Ӧ��CH4(g)��H2O(g) CO(g)��3H2(g)������CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ�� CO(g)��3H2(g)������CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
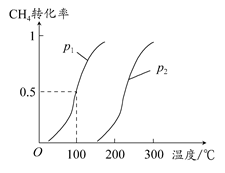
����֪100��Cʱ�ﵽƽ�������ʱ��Ϊ5 min������H2��ʾ��ƽ����Ӧ����Ϊ________��
��ͼ�е�p1________p2(�<����>������)��100��Cʱƽ�ⳣ��Ϊ________��
���������������������½����¶ȣ��淴Ӧ���ʽ�________(�������С�����䡱)��
(2)��ѹǿΪ0.1 MPa�����£�a mol CO��3a mol H2�Ļ�������ڴ������������Է���Ӧ���ɼ״���CO(g)��2H2(g) CH3OH(g)������ CH3OH(g)������
�ܸ÷�Ӧ�Ħ�H________0����S________0(�<����>������)��
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ���________��
A�������¶�
B����CH3OH(g)����ϵ�з���
C������He��ʹ��ϵ��ѹǿ����
D���ٳ���1 mol CO��3 mol H2
��Ϊ��Ѱ�Һϳɼ״����¶Ⱥ�ѹǿ������������ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��С������±��ո�������ʣ���ʵ���������ݡ�
ʵ����
| T(��C)
| n(CO)/n(H2)
| p(MPa)
| ��
| 150
| ??
| 0.1
| ��
| ________
| ________
| 5
| ��
| 350
| ________
| 5
?
4��ѡ���� ���淴Ӧ��2NO2?2NO+O2�ڹ̶�����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ�������
�ٵ�λʱ��������n?mol O2��ͬʱ����2n?mol NO2��
�ڵ�λʱ��������n?mol O2?��ͬʱ������2n?mol?NO��
����NO2��NO��O2?�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬��
�ܻ���������ɫ���ٸı��״̬��?
�ݻ��������ܶȲ��ٸı��״̬��
��������ƽ����Է����������ٸı��״̬��
A���٢ܢ�
B���ڢۢ�
C���٢ۢ�
D���٢ڢۢܢݢ�
5��ѡ���� һ���¶��£�ijһ�����ܱ��������п��淴Ӧ��A��g��+3B��g��
2C��g�����÷�Ӧ���е�һ���Ⱥ�ﵽ��ѧƽ��ı�־�ǣ�������
A����λʱ��������amol����A��ͬʱ����3amol����B
B��������������ܶȲ�����ʱ����ı�
C������C���������ʺͷֽ��������
D������A��B��C�ķ�����֮��Ϊ1��3��2
|
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772