微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知热化学方程式: H2O(g)=H2(g) +1/2O2(g)?△H = +241.8kJ/mol
H2(g)+ 1/2O2(g)=H2O(1)?△H =" -" 285.8kJ/mol
当1g液态水变为水蒸气时,其热量变化是????(??)
A.吸热44kJ
B.吸热2.44KJ
C.放热44kJ
D.放热2.44KJ
参考答案:B
本题解析:略
本题难度:简单
2、选择题 已知下列四个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g)?△H1;????? 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g)????△H3;?????2H2S(g)+O2(g)=2S(s)+2H2O(l) △H4;
则△H四者的关系中正确的是
A.△H1>△H2>△H3>△H4
B.△H4>△H2>△H3>△H1
C.△H3>△H4>△H1>△H2
D.△H4>△H3>△H2>△H1
参考答案:C
本题解析:
试题分析:H2S完全燃烧生成液体水时放出的热量最多,但放热越多,△H越小,因此最小△H2,其次是△H1;H2S不完全燃烧放出的热量少,其中生成气态水放热最少,所以△H3最大,其次是△H3,因此△H四者的关系中正确的是△H3>△H4>△H1>△H2,答案选C。
本题难度:一般
3、选择题 下列有关化学反应热的描述中,正确的是?????????????????????????????(????)
①化学反应过程中一定有能量变化;②△H>0表示放热反应,△H<0表示吸热反应;③△H的大小与热化学方程式中的化学计算数成正比;④放热反应在常温下就一定能进行;⑤生成物的总能量小于反应物总能量时,△H<0;⑥化学反应中放出的热才是反应热;
A.①③⑤
B.②④⑥
C.①②③
D.④⑤⑥
参考答案:A
本题解析:化学变化的特征之一就是伴随能量的变化。△H>0表示吸热反应,△H<0表示放热反应。在热化学方程式中物质前面的化学计量数表示的是参加反应的物质的物质的量,与反应热成正比。反应条件与反应是放热反应还是吸热反应无关。生成物的总能量小于反应物的总能量,反应是放热反应,△H<0。在化学反应过程中放出或吸收的能量都是反应热。答案是A。
本题难度:一般
4、选择题 中和热测定实验中,下列操作一定会降低实验准确性的是( )
A.用滴定管取所用药品
B.NaOH溶液在倒入小烧杯时,有少量溅出
C.大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多
D.测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度
参考答案:B
本题解析:NaOH溶液在倒入小烧杯时,有少量溅出,实验中生成水的量减少,放出的热量减小,测得中和热的数值不准。
本题难度:一般
5、填空题 (7分)反应A(g)+B(g)  ?C(g) +D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题。
?C(g) +D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题。
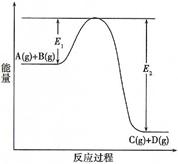
①?图中E1代表的意义是????????????。
该反应是?????????????反应(填“吸热”、“放热”)。反应热△H的表达式为???????????????。
②?当反应达到平衡时,升高温度,A的转化率???????????(填“增大”、“减小”或“不变”)。
③ 在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1??????, E2??????(填“增大”、“减小”或“不变”)。化学平衡?????????移动(填“向左”、“向右”或“不”)。
参考答案: 本题解析:略
本题解析:略
本题难度:一般