微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 用电除尘法可除去火力发电厂烟囱中大量的粉煤灰。已知粉煤灰的主要成分如下表,从粉煤灰中能够获得Al2O3。某校研究性学习小组设计了如图所示的提取Al2O3的工艺流程图。

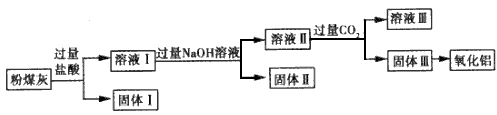
请回答下列问题。
(1)上述氧化物中能与NaOH溶液反应的是___。
(2)①固体I中含有的主要物质的化学式为__。
②向溶液Ⅱ中通人过量的CO2,发生反应的离子方程式为___。
(3)电解氧化铝制备金属铝时常常需加入冰晶石,冰晶石的作用是___,电解氧化铝的化学方程式为________,理论上从1t粉煤灰中可得到铝的质量为__。
参考答案:(1)SiO2.SO2和Al2O3
(2)①SiO2
本题解析:
本题难度:一般
2、选择题 当燃烧镁和某金属组成的合金时,所形成的氧化物的质量为反应前合金质量的2倍,则另一金属可能是(?????????)
A.铜
B.铍
C.钠
D.铝
参考答案:B
本题解析:由Mg生成MgO,质量增加的倍数小于1,则另一金属变为氧化物后质量增加的倍数应大于1,符合情况的为B。
本题难度:简单
3、选择题 除去镁粉中混有的少量铝粉,可选用的溶液是( )
A.盐酸
B.浓硝酸
C.氨水
D.氢氧化钠溶液
参考答案:A、镁粉、铝粉均能与稀盐酸反应,不但能把杂质除去,也会把原物
本题解析:
本题难度:简单
4、填空题 0℃,1.01×105Pa时,分别向甲、乙、丙三个容器中加入30.0mL同浓度的盐酸,
反应容器
| 甲
| 乙
| 丙
| ?
|
加入合金质量(g)
| 0.510
| 1.53
| 3.57
| ?
|
与盐酸反应生成气体(L)
| 0.560
| 0.672
| 0.672
| ?
|
与氢氧化钠反应产生气体(L)
| 0.336
| x
| y
| ?
?
再加入不同质量的由两种金属组成的合金粉末,测量放出气体的体积。若在甲、乙、丙三个容器中加入与盐酸同体积同浓度的氢氧化钠溶液,再分别加入与上述实验相同质量的同种合金,测量放出气体的体积,如下表:
根据表中数据可以计算得出的是_________;
A.合金的组成?????????? B.合金中组分的含量
C.盐酸的物质的量浓度?? D.盐酸的密度
能计算出的量的值为__________________;
(2)若两种金属是下列选项中的某两种,则从甲容器中的两次实验:
①不经计算,肯定没有________________(填字母符号);
A.40Ca??? B.56Fe??? C.64Cu??? D.24Mg??? E.27Al
②通过计算讨论推测合金的成分____________;
(3)根据(2)的推测结果,计算x和y的值分别为多少?
参考答案:(1)C??? 2mol/L???(2)①C???②Mg和A
本题解析:(1)由表中数据可知:甲中盐酸过量,丙中盐酸不足,则由丙中氢气的量可求出盐酸为0.06mol,进而求出盐酸的物质的量浓度为2mol/L。
(2)由题知:①中合金与盐酸、氢氧化钠溶液反应放出气体的量不等,则说明肯定没有与盐酸、氢氧化钠溶液都不反应的金属(即铜)存在;若存在铜,则另一金属与盐酸、氢氧化钠反应产生的氢气的量要么相等,要么有一个为0。
②合金中肯定有一种金属与氢氧化钠溶液反应,而另一种金属与氢氧化钠溶液不反应。能与氢氧化钠溶液反应放出氢气的只有选项中的Ca和Al。
若含有Ca:<
本题难度:简单
5、选择题 向含有a mol AlCl3的溶液中加入含b mol KOH的溶液,生成沉淀的物质的量可能是
(1)a mol(2)b mol(3)a/2 mol(4)b/2 mol(5)0 mol (6)(4a-b) mol(???)
A.(1)(2)(4)(5)(6)
B.(1)(3)(4)(5)(6)
C.(1)(2)(3)(5)(6)
D.只有(1)(3)(5)(6)
参考答案:D
本题解析:如果铝离子全部转化为氢氧化铝沉淀,则最多是amol。如果氢氧化钾过量,则得不到氢氧化铝沉淀。如果氢氧化钾不足,生成的氢氧化铝部分被溶解,则生成的氢氧化铝是b-3a-a=b-4a。如果氢氧化钾不足,溶液中还含有铝离子,则生成的氢氧化铝就小于amol,所以正确的答案选D。
本题难度:一般
|