微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 拉曼光谱证实溶液中不存在 ,实际存在[Al(OH)4]-。200 mL 0.2 mol?L-1 Na[Al(OH)4]溶液与250 mL 0.2 mol?L-1 H2SO4混合,完全反应后,溶液中Al3+与 物质的量之比为(??)
A.4:5
B.2:3
C.2:5
D.1:2
2、简答来源:91exam .org题 二氧化碳常被用作灭火剂,但是,当把点燃的镁条伸入盛有二氧化碳的集气瓶时,镁条却能继续燃烧,发出耀眼的白光,生成一黑一白两种物质.写出化学方程式,并用单线桥分析电子转移的数目______.
3、填空题 工业制备铝一般是从铝土矿(主要成分是Al2O3,含有杂质Fe2O3)中得到纯净的Al2O3,然后是电解
Al2O3得到铝。下图是从铝土矿中提纯是的简单示意图。其中牵涉到的一个反应是:
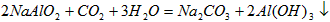
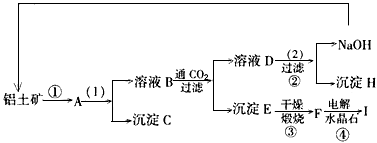
(1)写出图示中(1)的实验操作是______________;图示中(2)加入的试剂______________。
(2)试推断物质(写化学式)B_________;C_________;H__________;F____________。
(3)写出化学方程式: ①_______________________。④_______________________。
4、填空题 铝广泛应用于化学工业和日常生活中。工业上由铝土矿(Al2O3・3H2O的含量约为85%,其余主要为SiO2、Fe2O3等)冶炼金属铝的流程如下。
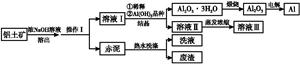
已知拜耳法生产Al2O3・3H2O的基本原理为:
Al2O3・3H2O+2NaOH(aq)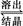 2NaAlO2(aq)+4H2O,[Al2O3・3H2O也可表示为2Al(OH)3]
2NaAlO2(aq)+4H2O,[Al2O3・3H2O也可表示为2Al(OH)3]
(1)操作Ⅰ的名称为 ,赤泥中除含有铝硅酸盐外,还含有的主要物质有??????????。
(2)为了提高铝土矿的溶出速率可采取的有效措施为?????????????????(任写三点)。
(3)用化学平衡理论解释稀释溶液Ⅰ有利于Al2O3・3H2O 结晶的原因 ??????????????。
(4)为了析出Al2O3・3H2O,也可向溶液Ⅰ中通入过量CO2气体,写出生成Al2O3・3H2O的离子方程式:?????????????????????????????????????????????????????????? 。
(5)为了回收赤泥附着液带走的有用成分,工业上将用热水洗涤后的洗液用作溶液Ⅰ的稀释剂,请指出流程图中另一处类似的做法 ???????????????????????????????????。
5、简答题 铝作为材料金属在现代社会中发挥着巨大的作用,铝的化合物在工农业生产及人们的日常生活中也具有广泛地作用。
(1)若将铝溶解,下列试剂中最好选用________(填编号)。
A.浓硫酸? B.稀硫酸? C.稀硝酸
(2)工业制备金属铝利用含有杂质氧化铁和二氧化硅的铝土矿(主要成分为氧化铝)为原料,先制备Al(OH)3。方法是先在铝土矿中加入硫酸,过滤,然后在滤液中加入过量的NaOH溶液,再过滤,在滤液中通入________(一种过量的气体),该反应的离子方程式_______________________________________________。
(3)工业上用电解熔融Al2O3的方法制备金属铝,其阴极反应式为_________。
(4)我国首创以铝、空气、海水为能源的新型电池。该电池以取之不尽的海水为电解液,靠空气中的氧气使铝不断氧化而产生电流。这种海水电池的能量比“干电池”高20~50倍。该新型电池用于航海标志灯已研制成功,只要把灯放入海水中数秒钟,就会发出耀眼的白光。该电池的总反应为:4Al+3O2+6H2O===4Al(OH)3。其负极材料为________,正极反应式为_________________。
(5)碱式氯化铝(分子式可表示为Al2(OH)nCl(6-n)是一种新型无机混凝剂,该产品对工业污水、造纸水、印染水具有较好的净化效果。为确定碱式氯化铝分子式中的n值,可采用沉淀称量法。准确称取碱式氯化铝样品4.97 g,配制成500 mL溶液,用硝酸酸化后,然后逐滴加入过量的AgNO3溶液。然后对沉淀进行过滤、洗涤、干燥,称取沉淀物质量为14.35 g。该碱式氯化铝中的n=________。