微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法中正确的是( )
A.摩尔既是物质的数量单位,又是物质的质量单位
B.物质的量既表示物质的数量又表示物质的质量
C.阿伏加德罗常数是12Kg12C中含有的碳原子数
D.1molH2O含有2molH和1molO
参考答案:D
本题解析:
本题难度:一般
2、选择题 下列溶液中,Cl-的物质的量浓度与50ml?1mol/LAlCl3溶液中Cl-物质的量浓度相等是( )
A.100ml1mol/LNaCl溶液
B.75ml1mol/LMgCl2溶液
C.150ml3mol/LKCl溶液
D.25ml2mol/LAlCl3溶液
参考答案:A、100ml1mol/LNaCl溶液中氯离子的物质的量浓度
本题解析:
本题难度:简单
3、选择题 向10 g Fe2O3、SiO2和Al2O3的混合物中,加入100 mL x mol/L稀硫酸,过滤后,向滤液中加入10 mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示。下列叙述错误的是( )
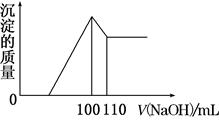
A.混合物和稀硫酸反应时,稀硫酸过量
B.可求出x的值
C.可求出Al2O3的质量分数
D.可求出Fe2O3的质量分数
参考答案:D
本题解析:由于SiO2不溶于稀硫酸,因此滤渣为SiO2。向滤液中加入NaOH溶液时,开始时无沉淀生成,说明稀硫酸过量,A正确。当沉淀的质量达到最大时,溶液中的溶质为Na2SO4,由此可得x=5,B正确。根据图像可知溶解Al(OH)3时消耗NaOH的物质的量为0.1 mol,则原混合物中n(Al2O3)为0.05 mol,由此可得Al2O3的质量分数为51%,C正确。由于图像中未给出向混合溶液中加入NaOH溶液时,过量的酸消耗NaOH的量,因此无法求出混合物中Fe2O3的质量分数,D错。
本题难度:一般
4、选择题 若以M表示水的摩尔质量,V表示在标准状况下水蒸气的摩尔体积,ρ为在标准状况下水蒸气的密度,NA为阿伏加德罗常数,m、Δ分别表示每个水分子的质量和体积,下面是四个关系式正确的是
A.NA=Vρ/m
B.ρ=M/(NAΔ)
C.m=M/NA
D.Δ=V/NA
参考答案:AC
本题解析:略
本题难度:一般
5、选择题 向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀总物质的量和加入溶液B的体积关系如图所示:
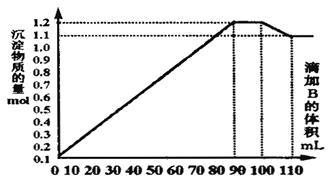
(1)当加入B溶液110 mL时,溶液中的沉淀是??????????????????(填化学式)
(2)将A.B溶液中各溶质的物质的量浓度填入下表:
溶?质
| Na2SO4
| BaCl2
| AlCl3
| FeCl3
|
/mol・L-1
| ?
| ?
| ?
| ?
?
(3)写出滴加B溶液90-100mL时的离子方程式:
?????????????????????????????????????????????????????????????????。
参考答案:(1)?? BaSO4?? Fe(OH)3 ?(填化学式)?
本题解析:
试题分析:分析各段线段的含义:加入B溶液0-90ml时,生成氢氧化铝、氢氧化铁和硫酸钡沉淀;90-100ml,生成硫酸钡沉淀,氢氧化铝溶解,而且二者物质的量相等;100-110ml,只有氢氧化铝溶解,所以(1)当加入B溶液110ml时,氢氧化铝已经溶解,沉淀为硫酸钡和氢氧化铁。(2)加入B溶液100-110ml,溶解了氢氧化铝0.1mol,则加入B溶液100-110ml时,也溶解了氢氧化铝0.1mol,生成硫酸钡0.1mol,可得氯化铝共0.2mol,C(AlCl3)=2mol・L-1,加入B溶液
本题难度:一般
|