��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij�¶��£���2 mol A��3 mol B����һ�ܱյ������з�����Ӧ��aA(g)+B(g) 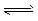 C(g)+D(g)��5 min���ƽ�⡣��֪�÷�Ӧ�ڴ��¶���ƽ�ⳣ��K��1�����¶Ȳ��������½��������������Ϊԭ����10����A��ת���ʲ������仯����B��ת����Ϊ
C(g)+D(g)��5 min���ƽ�⡣��֪�÷�Ӧ�ڴ��¶���ƽ�ⳣ��K��1�����¶Ȳ��������½��������������Ϊԭ����10����A��ת���ʲ������仯����B��ת����Ϊ
?[???? ]
A��40%
B��60%
C��24%
D��4%
�ο��𰸣�A
���������
�����Ѷȣ�һ��
2��ѡ���� ���ܱ������У�һ����������巢����Ӧ�� xA��g��+yB��g���PzC��g��ƽ��ʱ���A��Ũ��Ϊ0.50 mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ�Ƚ���Ϊ0.30 mol/L�������й��ж���ȷ���ǣ�??����
A��x+y<z
B��ƽ��������Ӧ�����ƶ�
C��B��ת��������
D��C����������½�
�ο��𰸣�D
����������������ݻ�����ԭ����������˲�䣬A��Ũ��Ӧ��0.25 mol/L.��ƽ���A��Ũ����0.30 mol/L��˵����Сѹǿ��ƽ��������Ӧ�����ƶ���������Ӧ���������Ŀ��淴Ӧ������ѡ��D����ȷ�ģ�����Ǵ���ģ���ѡD��
�����Ѷȣ�һ��
3��ѡ���� ��һ���¶������£��ס��������ݻ���ȵĺ����ܱ������о��������·�Ӧ��3A��g��+B(g)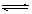 XC(g)+D(S)�������ͨ��6molA��2molB��������ͨ��1.5molA��0.5molB��3molC��2molD����Ӧһ��ʱ��ﵽƽ�⣬��ʱ��ļס������������е�C�������������0.2��������������ȷ���ǣ�
XC(g)+D(S)�������ͨ��6molA��2molB��������ͨ��1.5molA��0.5molB��3molC��2molD����Ӧһ��ʱ��ﵽƽ�⣬��ʱ��ļס������������е�C�������������0.2��������������ȷ���ǣ�
A��ƽ��ʱ���е�A���������Ϊ0.4
B��ƽ��ʱ�ס������������е�A��B�����ʵ���֮�Ȳ����
C����ƽ��ʱ�������е�ѹǿ����ȣ����������е�ѹǿ֮��Ϊ8:5
D����ƽ��ʱ�ס����������е�A�����ʵ�����ȣ���x=4
�ο��𰸣�C
���������
�������������Ϊ��Чƽ�⣬�õ�Чƽ���������������x=4��Ϊ�ȱȵ�Ч����x=2Ϊ���ϵ�Ч����ȫ��Ч����A�����������������B������C����ƽ��ʱ�������е�ѹǿ����ȣ�ӦΪ��һ�����������ѹǿ�ȵ������ʵ����ȣ�����ת��Ϊ��Ӧ�����5mol�����������е�ѹǿ֮��Ϊ8:5����ȷ��D������
�����Ѷȣ�һ��
4��ѡ���� һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״���
������ΪCu2O/ZnO����CO(g)��2H2(g)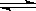 CH3OH(g)���״������ʵ������¶ȵĹ�ϵ����ͼ��ʾ�����з�����ȷ����????��?????��??????????????????????????????????????????????????????????????
CH3OH(g)���״������ʵ������¶ȵĹ�ϵ����ͼ��ʾ�����з�����ȷ����????��?????��??????????????????????????????????????????????????????????????

A����Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽ K��c(CH3OH)/c(CO)��c2(H2)
B�������¶ȣ�Kֵ����
C����500�棬�ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)��3tB /2nB mol��(L��min)��1
D�������������䣬E������ѹ����ԭ����1/2������ƽ��ʱn(H2)/n(CH3OH)����
�ο��𰸣�A
�����������
�����Ѷȣ���
5��ѡ���� ��1 mol CO��2 mol H2����һ�ݻ�Ϊ1L���ܱ������У��ֱ���250��C��T��C�·�����Ӧ:CO(g)+2H2(g)��CH3OH(g)����H="a" kJ/mol,��ͼ�����з�������ȷ����

A��250��Cʱ��0?10minH2��Ӧ����Ϊ 0.015 mol,/(L.min)
B��ƽ��ʱCO��ת���ʣ�T��ʱС��250��ʱ
C�������������䣬����С�ݻ������CO�����������
D��a<0,ƽ�ⳣ��K:T0Cʱ����2500C
�ο��𰸣�D
���������
��������� A��250��Cʱ��0?10min CH3OH��Ӧ����Ϊ0.015 mol/(L��min)������������Ӧ����Ϊ0.03mol/(L��min)������B����ͼ���֪��250��ʱ��Ӧ���ʿ죬��ƽ��ʱ�״����ʵ���С��˵������Ӧ�Ƿ��ȷ�Ӧ���¶�Խ�ͣ�COת����Խ����C����С���������Ч������ѹǿ��ƽ��������Ӧ�����ƶ���CO���������С������D������Ӧ�Ƿ��ȷ�Ӧ��a<0���¶�Խ�ͣ�ƽ�ⳣ��Խ����ȷ��
�����Ѷȣ���