微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于可逆反应:2SO2(g)+O2(g)?2SO3(g)△H<0,下列研究目的和示意图相符的是( )
| ? | A | B | C | D
研究目的
压强对反应的影响
(p2>p1)
温度对反应的影响
平衡体系增加O2的浓度对反应的影响
体积恒定的密闭容器中催化剂对反应的影响
图示
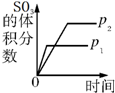
?
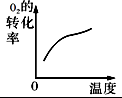
?
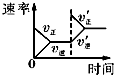
?
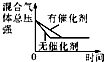
?
A.A
B.B
C.C
D.D
参考答案:A.增大压强,反应速率增大,到达平衡所用时间较少,图象不符,
本题解析:
本题难度:一般
2、选择题 反应①:Fe(s)+CO2(g) FeO(s)+CO(g) △H>0 FeO(s)+CO(g) △H>0
反应②:Fe(s)+H2O(g)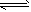 FeO(s)+H2(g) △H<0 FeO(s)+H2(g) △H<0
若反应①在温度T1下进行,反应②在温度T2下进行,已知T1>T2,且c(CO2)>c(H2O)(其他条件均匀相同),下面对两者反应速率大小判断正确的是 [???? ]
A. 反应①快
B. 反应②快
C. 一样快
D. 无法判断
参考答案:D
本题解析:
本题难度:一般
3、实验题 (12分)某同学为了探究锌与硫酸反应过程中的速率变化,他在100mL稀硫酸中加入足量的锌粉,标况下用排水集气法收集反应放出的氢气,实验记录如下(累计值):
时间(min)
| 1
| 2
| 3
| 4
| 5
| 氢气体积(mL)(标准状况)
| 50
| 120
| 232
| 290
| 310
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大______________,原因是______________________________________________。
(2)哪一时间段的反应速率最小________________,原因是___________________。
(3)求2~3分钟时间段以硫酸的浓度变化来表示的该反应速率(设溶液体积不变,要写出计算过程)______________________________________________________。
(4)该同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
①上述实验中涉及到的离子反应方程式有????????????????????????????????????????????
??????????????????????????????????????;
②硫酸铜溶液可以加快氢气生成速率的原因是???????????????????????????????;
③实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与实验中CuSO4??溶液起相似作用的是?????????????????;
④该同学通过实验进一步研究了硫酸铜的量对氢气生成速率的影响。该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
??????????????????????????????????????????。
参考答案:(1) 2~3min(1分),温度对反应速率影响占主导作用(
本题解析:(1)根据表中数据可知,在0~1、1~2、2~3、3~4、4~5min内收集到的氢气分别是(ml)50、70、112、58、20。所以2~3min内反应速率最大,这是由于反应是放热反应,温度对反应速率的影响超过了浓度对反应速率的影响。
(2)4~5min内收集到的气体最少,所以反应速率最小。这是由于随着反应的进行,反应物
的浓度减小,此时浓度对反应速率的影响超过了温度对反应速率的影响。
(3)略
(4)加入硫酸铜后,新可以置换出铜,从而构成铜锌原电池,锌作负极,加快反应速率。有
本题难度:一般
4、选择题 影响化学反应速率的因素很多,下列措施一定能使化学反应速率增大的是 [???? ]
A.升高温度
B.增大压强
C.降低浓度
D.减小压强
参考答案:A
本题解析:
本题难度:一般
5、选择题 某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示.下列说法中正确的是( )

A.30min时降低温度,40min时升高温度
B.反应方程式中的x=1,正反应为吸热反应
C.8min前A的平均反应速率为0.08mol/(L?min)
D.30min~40min间该反应使用了催化剂
参考答案:A.由图象可知,30min时正、逆反应速率降低了,反应物与生
本题解析:
本题难度:简单
|
|